将适量铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和生成的Fe2+物质的量之比为
| A.1:1 | B.1:2 | C.2:3 | D.2:1 |
要使含有Ag+、Cu2+、Mg2+、Ba2+等离子的溶液中的离子逐一形成沉淀析出,下列所选择试剂及加入试剂的顺序正确的是
| A.H2SO4→HCl→K2S→NaOH→CO2 | B.Na2SO4→NaCl→Na2S→NH3·H2O |
| C.NaCl→Na2SO4→H2S→NaOH | D.Na2S→Na2SO4→NaCl→NaOH |
M是一种治疗艾滋病的新药(结构简式见下图),已知M分子中—NH—COO—(除H外)与苯环在同一平面内,关于M的以下说法正确的是 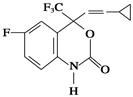
| A.该物质易溶于水 | B.M的分子式为C13H12O2NF4 |
| C.M能发生加聚反应 | D.M分子内至少有13个碳原子在同一平面内 |
所谓“绿色汽车”是指使用液化石油气作能源的汽车。绿色汽车可避免有毒的铅、苯的同系物以及稠环芳烃的排放。燃烧等质量的液化石油气(主要成分是含C3—C4的烷烃)与汽油(主要成分是含C5—C11的烷烃)相比较
| A.液化石油气生成的水少 | B.液化石油气消耗氧气量少 |
| C.液化石油气燃烧产生的热量少 | D.液化石油气产生的含碳化合物少 |
下列各组离子在指定溶液中能大量共存的是
①常温下,c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+
②加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-
③中性溶液:Fe3+、Al3+、NO3-、SO42-
④使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl-
⑤无色溶液中:K+、Al3+、NO3-、HCO3-
| A.① | B.①③ | C.②③ | D.①④⑤ |
NA为阿伏加德罗常数,下列说法正确的是
| A.标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| B.28g乙烯所含共用电子对数目为4NA |
| C.1mol 苯中含有碳碳双键的数目为3 NA |
| D.2.8g聚乙烯中含有的碳原子数为0.2 NA |