碘盐中添加的碘酸钾在工业上可用电解KI溶液制取,电极材料是石墨和不锈钢,化学方程式是:KI+3H2O KIO3+3H2↑,有关说法不正确的是
KIO3+3H2↑,有关说法不正确的是
| A.石墨作阳极,不锈钢作阴极 |
| B.I-在阳极放电,H+在阴极放电 |
| C.电解过程中电解质溶液的pH变小 |
| D.电解转移3 mol e-时,理论上可制得KIO3 107 g |
下列表示物质结构的化学用语或模型图正确的是()
常温下有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的HCl溶液;③pH=11的氨水;④pH=11的NaOH溶液。下列说法正确的是
| A.①与②中c(H+)相同 |
| B.①与④混合,所得混合液的PH等于7 |
| C.②和③混合,所得混合溶液的pH大于7 |
| D.③与④分别用等浓度的盐酸中和,消耗盐酸的体积相等 |
银锌(Ag—Zn)可充电电池广泛用做各种电子仪器的电源,电解质为KOH。其电池总反应为:Ag2O + Zn + H2O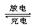 2Ag + Zn(OH)2,则下列说法正确的是
2Ag + Zn(OH)2,则下列说法正确的是
| A.放电时Ag2O参与反应的电极为负极 |
B.放电时 负极附近的pH逐渐减小 负极附近的pH逐渐减小 |
| C.充电时阴极的电极反应为:Zn(OH)2 + 2e-= Zn + 2OH- |
| D.充电时每生成1 mol Ag2O转移1 mol电子 |
下列说法正确的是
| A.乙醇和乙酸都能与氢氧化钠溶液反应 | B.乙烯和苯都能发生加成反应 |
| C.淀粉和蛋白质水解产物都是氨基酸 | D.葡萄糖和蔗糖都可发生银镜反应 |
在容积不变的密闭容器中进行反应:2SO2 ( g )+O2( g)  2SO3(g ) ;△H < O。下列各图表示当
2SO3(g ) ;△H < O。下列各图表示当 其它条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
其它条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
| A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻通人氦气对反应速率的影响 |
| C.图Ⅱ表示t0时刻使用催化剂对反应速率的影响 |
| D.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |