常温下,浓度均为0.1 mol/L的4种钠盐溶液pH如下:
| 溶质 |
Na2CO3 |
NaHCO3 |
NaClO |
NaHSO3 |
| pH |
11.6 |
9.7 |
10.3 |
5.2 |
下列说法不正确的是
A.四种溶液中,Na2CO3溶液中水的电离程度最大
B.NaHSO3溶液显酸性的原因是: NaHSO3 =Na+ + H+ + SO32-
C.向氯水中加入少量NaHCO3(s),可以增大氯水中次氯酸的浓度
D.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3
下列实验装置能达到相关实验目的的是()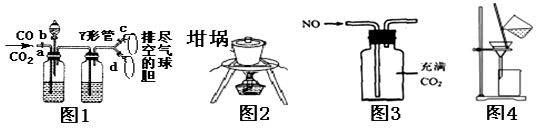
| A.图1可用于分离收集CO和CO2 |
| B.图2可用于从食盐水中提取NaCl晶体 |
| C.图3用于收集NO |
| D.图4用于氢氧化铁胶体和硫酸钠溶液的分离 |
NA代表阿伏加德罗常数的值,下列有关叙述不正确的是()
| A.在熔融状态下,1molNa2O2完全电离出的离子数目为3NA |
| B.将CO2通过Na2O2使固体质量增加mg,反应中转移的电子数m NA /14 |
| C.在标准状况下,22.4LCH4与18 gH2O所含有的电子数均为10NA |
| D.含1mol Cl-的NH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液中NH4+数为 NA |
下列解释事实的化学方程式或离子方程式不正确的是()
| A.向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2=I2+2H2O |
| B.自然界各种原生铜的硫化物经氧化、淋滤作用后产生的硫酸铜,遇到难溶液的PbS,慢慢转变为铜蓝(CuS):Cu2++SO42-+PbS═CuS+PbSO4 |
| C.在燃煤时加入适量石灰石,可减少SO2的排放:2CaCO3+O2+2SO2═2CaSO3+2CO2 |
| D.在盐碱地(含较多NaCl、Na2CO3)上通过施加适量CaSO4,可降低土壤的碱性:CaSO4+Na2CO3═CaCO3↓+Na2SO4 |
分子式为C9H12O属于芳香醇且苯环上有三个取代基的同分异构体共有()
| A.4种 | B.5种 | C.6种 | D.8种 |
化学与人类生活密切相关,下列与化学有关的说法不正确的是()
| A.化石燃料燃烧和工业废气中的氢氧化物均是导致“雾霾天气”的元凶 |
| B.开发和推广新能源是实现低碳生活的途径之一 |
| C.粮食酿酒主要经过了淀粉→葡萄糖→乙醇的化学变化过程 |
| D.化学药品着火,都要立即用水或泡沫灭火器灭火 |