用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B.1.5 mol NO2与足量H2O反应,转移的电子数为2NA |
| C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.标准状况下,22.4 L己烷中共价键数目为19NA |
某溶液可能含有Cl-、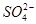 、
、 、NH+ 4、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
、NH+ 4、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
| A.NH+ 4Fe3+一定存在, K+可能存在 |
| B.Cl−一定存在,且c(Cl−)≤0.4 mol/L |
C.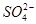 、NH+ 4Fe3+一定存在,且物质的量浓度均为0.02 mol/L 、NH+ 4Fe3+一定存在,且物质的量浓度均为0.02 mol/L |
D. 、Al3+一定不存在,K+一定存在 、Al3+一定不存在,K+一定存在 |
第三周期主族元素W、X、Y、Z,其简单离子都能促进水的电离平衡的是()
| A.W2—、X+ | B.Y3+、Z2— | C.X+、Y3+ | D.X2+、Z— |
下列表示对应化学反应的离子方程式正确的是()
| A.Fe3O4与足量稀HNO3反应: Fe3O4+8H+=2Fe3++Fe2++4H2O |
| B.用小苏打治疗胃酸过多:NaHCO3+H+=Na++CO2↑+H2O |
| C.双氧水中加入稀硫酸和KI溶液:H2O2 + 2H+ + 2I- = I2 + 2H2O |
| D.往碳酸氢钙溶液中滴入少量氢氧化钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+ 2H2O + CO32- |
设NA为阿伏加德罗常数。下列说法正确的是
| A.1L 1mol·L-1的NaClO 溶液中含有ClO-的数目为NA |
| B.1mol Mg在空气中燃烧被完全氧化生成MgO和Mg3N2,失去2 NA个电子 |
| C.标准状况下,22.4L苯含有1 NA个苯分子 |
| D.1mol的羟基与1mol的氢氧根离子所含电子数均为9 NA |
下列物质分类正确的是
| A.SO2、SiO2、 CO均为酸性氧化物 |
| B.稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C.烧碱、冰醋酸、四氯化碳均为电解质 |
| D.福尔马林、水玻璃、氨水均为混合物 |