下列根据实验操作和现象所得出的结论正确的是:
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
向溶液中滴加盐酸酸化的BaCl2溶液 |
产生白色沉淀 |
溶液中一定含有SO42- |
| B |
向溶液X中先滴加稀NaOH溶液,再将湿润红色石蕊试纸置于试管口附近 |
试纸不变蓝 |
原溶液中无NH4+ |
| C |
向PbO2中滴入浓盐酸 |
有黄绿色气体 |
PbO2具有氧化性 |
| D |
向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 |
有白色沉淀生成 |
溶液X中一定含有CO32- |
下列化学反应的离子方程式正确的是
| A.用稀HNO3溶解FeS固体:FeS+2H+===Fe2++H2S↑ |
| B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-===CaSO3↓+2HClO |
| C.在稀氨水中通入过量CO2:NH3·H2O+CO2===NH+HCO |
| D.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO===CaSO4↓+H2O |
短周期主族元素A、B、C、D,原子序数依次增大。A.C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是
A.原子半径:A<B<C<D B.单质B常温下能溶于浓硝酸
C.最高价氧化物对应水化物的酸性:D<C D.非金属性:A>C
油脂是多种高级脂肪酸的甘油脂。油脂的下列叙述和用途中,与其含有不饱和的碳碳双键有关的是
| A.油脂是产生能量最高的营养物质 |
| B.利用油脂在碱性条件下水解(皂化反应 cellulose)可以制得甘油和肥皂 |
| C.植物油经过氢化(加氢),可以变成脂肪 |
| D.油脂是有机体组织里储存能量的重要物质 |
在一密闭容器中进行反应:2SO2(g)+O2(g) 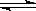 2SO3(g)测得开始时,SO2、O2、和SO3的浓度分别为0.2mol∙L-1、0.1mol∙L-1、0.2mol∙L-1,在反应过程中不断测该容器中各物质的浓度,下列测定数据肯定不正确的是
2SO3(g)测得开始时,SO2、O2、和SO3的浓度分别为0.2mol∙L-1、0.1mol∙L-1、0.2mol∙L-1,在反应过程中不断测该容器中各物质的浓度,下列测定数据肯定不正确的是
| A.O2为0.15mol∙L-1 | B.SO2为0.25mol∙L-1 |
| C.SO3为0.4mol∙L-1 | D.O2、SO3的浓度相等 |
对于敞口容器中的反应:Zn(s)+H2SO4(aq)= ZnSO4 (aq)+H2(g), 反应过程中能量关系可用如图表示,下列叙述中不正确的是()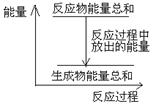
| A.1 molZn的能量高于1 molH2的能量 |
| B.用锌粉代替锌粒,速率会加快 |
| C.如果Zn足量,反应速率会经历由慢到快到慢的过程 |
| D.反应物Zn和H2SO4的总能量高于产物 ZnSO4和H2的总能量 |