下列离子方程式错误的是
| A.向碳酸氢镁溶液中加人过量氢氧化钠:Mg2++2HCO3-+2OH-→MgCO3↓+2H2O+ CO32- |
| B.Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+→2Fe3++3H2O |
| C.向NH4HSO4溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:Ba2+ + 2OH-+ NH4+ +H+ + SO42-→BaSO4↓+ NH3·H2O + H2O |
| D.大理石溶于醋酸:CaCO3 + 2CH3COOH →Ca2+ + 2CH3COO—+ H2O + CO2↑ |
用丙醛(CH3-CH2-CHO)制取聚丙烯的过程中发生的反应类型依次为()
①取代 ②加成 ③消去 ④氧化 ⑤还原 ⑥加聚 ⑦缩聚
| A.①④⑥ | B.⑤②⑦ | C.⑤③⑥ | D.②④⑤ |
亚油酸通常为淡黄色透明液体,能降低血脂,降低血清中胆固醇含量,防止动脉粥样硬化,主要来源于豆油、花生油、棉籽油和亚麻仁油,其结构简式为CH3(CH2)3(CH2CH=CH) 2(CH2)7COOH。下列说法中正确的是( )
| A.亚油酸是一种植物油,常温下呈液态 | B.1mol亚油酸可以与3molH2反应 |
| C.亚油酸能使溴的四氯化碳溶液褪色 | D.亚油酸可与NaOH溶液发生皂化反应 |
褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到。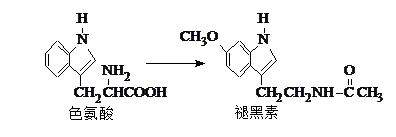
下列说法不正确的是( )
| A.色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点 |
| B.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出 |
| C.在一定条件下,色氨酸可发生缩聚反应 |
| D.褪黑素与色氨酸结构相似,也具有两性化合物的特性 |
下列化学方程式或离子方程式,书写规范、正确的是(反应条件略)( )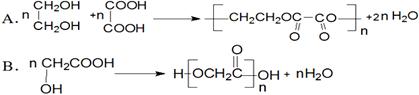
C.苯酚钠溶液中通入少量二氧化碳的离子方程式: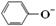 +H2O+CO2
+H2O+CO2
 +HCO3—
+HCO3—
D.乙酸与碳酸钠溶液反应的离子方程式:2H+ + CO32—= CO2↑ + H2O
在H2O、C6H5OH、 、CH3COOH、HCl的排列中,
、CH3COOH、HCl的排列中, 内应填入的物质是()
内应填入的物质是()
| A.H2CO3 | B.CH3COOCH3 | C.CH3CH2OH | D.H2SO4 |