(本题共12分)空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下: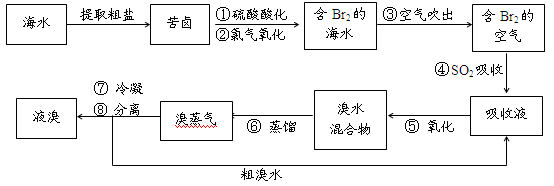
41、溴在元素周期表中位于_________周期,_________族。
42、步骤①中用硫酸酸化可提高Cl2的利用率,其原因是 。
43、步骤④的离子方程式:_______________________________________。
44、步骤⑥的蒸馏过程中,溴出口温度要控制在80—90℃。温度过高或过低都不利于生产,请解释原因:__________________________________________。
45、步骤⑧中溴气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是_____________,分离时液溴从分离器的_____(填“上口”或“下口”)排出。
46、不直接用步骤②后含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氧化”的原因是 。
47、下列有关溴单质的叙述正确的是
| A.是易挥发的深红棕色液体 |
| B.实验室少量液溴可保存在橡皮塞的棕色瓶中,并且加少量的水液封 |
| C.可用酒精从溴水中萃取溴 |
| D.溴可以与NaI溶液反应,置换出碘单质 |
已知下图中H是无色液体,号称生命之源,B是空气中含量最多的物质,E是红棕色气体。
(1)C的化学式是。
(2)D和E都是大气污染物,两种物质相互转化的化学方程式分别是:
①D→E。
②E→D。
(3)E和H的反应中,氧化剂和还原剂的质量比是。
(4)C和F反应生成G的化学方程式是。
(1)下列两组无色溶液分别选用一种试剂鉴别,写出试剂的化学式。
①NaCl Na2CO3 Na2SiO3 Na2SO3试剂:
②(NH4)2SO4 NH4C1 Na2SO4 NaCl试剂:
(2)下列物质中含有少量杂质(括号内物质为杂质),用离子方程式表示除去杂质的原理
| 编号 |
物质 |
离子方程式 |
| ① |
NaHCO3(Na2CO3) |
|
| ②[ |
SiO2(CaCO3) |
|
| ③ |
Fe2O3(Al2O3) |
|
| ④ |
FeCl2(FeCl3) |
写出下列反应的化学方程式
(1)过氧化钠与二氧化碳:
(2)二氧化硫与氧气:
(3)铜与浓硫酸:(标出电子转移的方向和数目)
(12分) 10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
| pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度(填“大于”或“小于”)NaHCO3。丙同学认为甲、乙的判断都不充分。丙认为:
⑴只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则(填“甲”或“乙”)判断正确。试剂X是。
A. Ba(OH)2溶液 B. BaCl2溶液 C. NaOH溶液 D. 澄清的石灰水
⑵将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则(填“甲”或“乙”)判断正确。
⑶查阅资料,发现NaHCO3的分解温度为150℃,丙断言(填“甲”或“乙”)判断是错误的,理由是。
250C时,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因(用离子方程式表示);
(2)混合溶液中由水电离出的c(H+)0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);(填>、<、=)
(3)求出混合液中下列算式的计算结果(填具体数字):
c (HA)+c (A-)=mol·L-1;
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH7 (填>、<、=);
(5)将相同温度下相同浓度的四种盐溶液:
A.NH4HCO3 B.NH4AC.(NH4)2SO4 D.NH4Cl
按pH由大到小的顺序排列(填序号)