NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.在密闭容器中加入l.5mol H2和0.5molN2,一定条件下充分反应后可得到NH3分子数为NA |
| B.一定条件下, 2.3g的Na完全与O2反应生成 3.6g产物时失去的电子数为0.1NA |
| C.1.0L 0.1 mol·L-1Na2S溶液中含有的S2-离子数为0.1NA |
| D.C2H4和C3H6混合物的质量a g,完全燃烧时消耗的O2一定是 33. 6a/14L |
酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性④乙醇是烃的含氧化合物
| A.②④ | B.②③ | C.①③ | D.①④ |
有关 分子结构的下列叙述中正确的是
分子结构的下列叙述中正确的是
①除苯环外的其余碳原子有可能都在一条直线上
②除苯环外的其余碳原子不可能都在一条直线上
③12个碳原子不可能都在同一平面上
④12个碳原子有可能都在同一平面上
| A.①② | B.②③ | C.①③ | D.②④ |
下列各组液体混合物,可以用分液漏斗分离的是
| A.乙醇和水 | B.溴乙烷和水 |
| C.溴乙烷和氯仿 | D.苯和溴苯 |
在核磁共振氢谱中出现两组峰,且其面积之比为3∶2的化合物是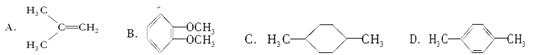
要从乙酸的乙醇溶液中回收乙酸,合理的操作组合是
①蒸馏②过滤③静止分液④加足量钠 ⑤加入足量H2SO4
⑥加入足量NaOH溶液⑦加入乙酸与浓H2SO4混合液后加热 ⑧加入浓溴水
| A.⑦③ | B.⑧⑤② | C.⑥①⑤② | D.⑥①⑤① |