(12分)数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果。
已知:C(s)+O2(g)=CO2(g);ΔH=-393 kJ·mol-1
2CO (g)+O2(g)=2CO2(g);ΔH=-566 kJ·mol-1
2H2(g)+O2(g)=2H2O(g);ΔH=-484 kJ·mol-1
(1)工业上常采用将水蒸气喷到灼热的炭层上实现煤的气化(制得CO、H2),该反应的热化学方程式是 。
(2)上述煤气化过程中需向炭层交替喷入空气和水蒸气,喷入空气的目的是 。
(3)CO常用于工业冶炼金属,下图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg[c(CO)/c(CO2)]与温度(t)的关系曲线图。
下列说法正确的是 。
A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属铬(Cr)
C.工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率
D.CO还原PbO2的反应ΔH>0
(4)某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A H++HA-,HA-
H++HA-,HA- H++A2-。已知相同浓度时的电离程度H2A>HA-,设有下列四种溶液:
H++A2-。已知相同浓度时的电离程度H2A>HA-,设有下列四种溶液:
A.0.01mol/L的H2A溶液;
B.0.01mol/L的NaHA溶液;
C.0.02mol/L的HCl与0.04mol/L的NaHA溶液等体积混合液;
D.0.02mol/L的NaOH与0.02 mol/L的NaHA溶液等体积混合液。
据此,填写下列空白(填代号)
(1)c(H+)最大的是 ,最小的是 ;
(2)c(H2A)最大的是 ,最小的是 ;
(3)c(A2-)最大的是 ,最小的是 。
A、B、C、D、E是中学化学中常见的无色气体,它们均由短周期元素组成。A、B、C相互转化关系如图所示(部分产物已略去)。已知: A能使湿润的红色石蕊试纸变蓝;C、D为空气中的主要成分;B、E是有毒气体,都能和血红蛋白结合。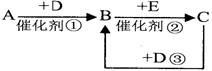
回答下列问题:
(1)A的结构式,C的电子式。
(2)下列气体实验室制取装置与用氯化铵和碱石灰加热制取A的装置相同的是(填序号)。
①氧气②氯气③氢气④二氧化碳
(3)反应②可用于汽车加装尾气催化净化装置,可以使B和E转化成无毒的气体,试写出反应②的化学方程式:。
(4)反应①的化学方程式:。
①14N②金刚石③14C④乙醇(CH3CH2OH)⑤13C⑥二甲醚(CH3OCH3)
(1)和互为同位素(填序号)
(2)和的质量数相同,质子数不同。(填序号)
(3)④和⑥互为。
(4)②金刚石属于晶体,熔化时需要克服微粒间的作用力是。
A、B、C、D、E是位于短周期的主族元素。已知:
①热稳定性:HmD>HmC;
②Cm-、E(m-1)-具有相同的电子层结构;
③A、B与C在同一周期,在该周期元素中,A的原子半径最大,B的离子半径最小;
④A与B质子数之和是D质子数的3倍。
依据上述信息用相应的化学用语回答下列问题:
考查原子核外电子的排布规律及元素周期律等。
(1)HmDm的电子式为
(2)Cm-、E(m-1)-的还原性强弱顺序为:_________,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________。
(3)B单质与A的最高价氧化物对应水化物反应的化学方程式为:______________________。
(4)常温下,将CDm通入HmC溶液中,有C析出,写出该过程的化学方程式。
(5)在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。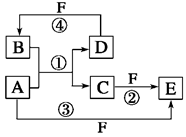
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A 是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A原子的结构示意图为,反应④的化学方程式为_______________。
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①和②均在水溶液中进行,写出反应②的离子方程式_________,E与A再生成C的离子方程式是。
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为___________________________________。
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为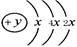 ;B、C可形成离子化合物B3C2,
;B、C可形成离子化合物B3C2,
据此利用相应的化学用语填空:
(1)A元素在周期表中的位置是,其气态氢化物的化学式为。
(2)A、B、C、D四种元素的原子半径由小到大的顺序为。
(3)B和C最高价氧化物对应水化物的化学式分别为和。