用CO合成甲醇的方程式为:CO(g) + 2H2(g)  CH3OH(g) △H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
CH3OH(g) △H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是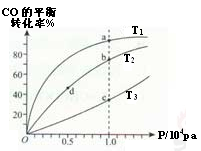
| A.温度:T1>T2>T3 |
| B.平衡常数:K(a)>K(c) 、K(b)=K(d) |
| C.反应速率:υ(a)>υ(c)、υ(b)>υ(d) |
| D.平均摩尔质量:M(a)<M(c) 、M(b)>M(d) |
如下图,各烧杯中盛有海水,铁在其中被腐蚀的速度由快到慢的顺序为 ( )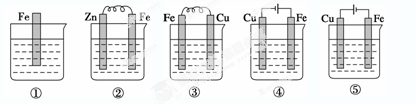
| A.①②③④⑤ | B.④③②①⑤ | C.④③①②⑤ | D.④②③①⑤ |
下列说法或表示方法正确的是( )
| A.已知C(s)+O2(g)=CO2(g) ΔH1,C(s)+1/2O2(g)="CO(g)" ΔH2;则ΔH1>ΔH2 |
| B.等量的H2在O2中完全燃烧,生成气态水比生成液态水放出的热量多 |
| C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
| D.由石墨比金刚石稳定可知:C(金刚石, s)=C(石墨, s) ΔH >0 |
下列有关吸热反应、放热反应的叙述中,正确的是 ( )
①如果反应物的总能量低于生成物的总能量,该反应一定是吸热反应。
②只要是在加热条件下进行的反应,一定是吸热反应
③只要是在常温常压下进行的反应,一定是放热反应
④中和反应和燃烧反应都是放热反应
⑤化合反应都是放热反应
⑥原电池反应可能是放热反应,也可能是吸热反应
| A.①④ | B.①②③ | C.④⑤⑥ | D.①④⑤⑥ |
2012年是勒夏特列诞生192周年,下列叙述中,不用平衡移动原理解释的是 ( )
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.高压比常压有利于合成SO3的反应 |
| C.由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| D.黄绿色的氯水光照后颜色变浅 |
已知充分燃烧a g乙炔气体时生成1 mol二氧化碳气体和液态水,并放出热量为b kJ,则乙炔燃烧的热化学方程式正确的是( )
| A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-4b kJ·mol-1 |
| B.C2H2(g)+5/2 O2(g)=2CO2(g)+H2O(l)ΔH="2b" kJ·mol-1 |
| C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-2b kJ·mol-1 |
| D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH="b" kJ·mol-1 |