已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是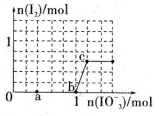
| A.还原性:HSO3->I-,氧化性:IO3->I2>SO42- |
| B.a点处的氧化产物是SO42-,还原产物是I- |
| C.当溶液中的I-为0.4mol时,加入的KIO3一定为0.4mol |
| D.若向KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为:2IO3-+5HSO3-=I2+5SO42-+3H++H2O |
下列叙述正确的是()
| A.2 mol NaOH的摩尔质量为80g/mol |
| B.NH4+的摩尔质量为17 g/mol |
| C.常温常压下,32g SO2含有的分子数约为3.01×1023 |
| D.2mol/L的CaCl2溶液中Cl-的数目为2NA |
某实验小组学生用50 mL 0.50 mol·L-1的盐酸与50 mL 0.50 mol·L-1的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算反应热.下列说法正确的是( )
| A.如图条件下实验过程中没有热量损失 |
| B.图中实验装置缺少环形玻璃搅拌棒 |
| C.烧杯间填碎纸条的作用是固定小烧杯 |
| D.若改用50 mL 0.50 mol·L-1的盐酸跟50 mL 0.50 mol·L-1的KOH溶液进行反应,从理论上说所求反应热不相等 |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是:
| A.反应达到平衡时,y的转化率为75% |
B.反应可表示为X+3Y 2Z,其平衡常数为1600 (mol·L-1)-2 2Z,其平衡常数为1600 (mol·L-1)-2 |
| C.增大压强使平衡向生成Z的方向移动,平衡常数不变 |
| D.改变温度或向平衡体系中加入X都会使平衡移动,平衡常数也会随之改变 |
现有下列两个图象:
下列反应中符合上述图象的是( )
A.N2(g)+3H2(g)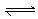 2NH3(g) ΔH<0 2NH3(g) ΔH<0 |
B.2SO3(g) 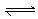 2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
C.4NH3(g)+5O2(g)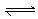 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
D.H2(g)+CO(g) 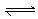 C(s)+H2O(g) ΔH>0 C(s)+H2O(g) ΔH>0 |
反应L(s)+aG(g) bR(g)达到平衡时,温度和压强对该反应的影响如图所示,
bR(g)达到平衡时,温度和压强对该反应的影响如图所示,
图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断 ( )
| A.上述反应正方向是放热反应 | B.上述反应正方向是吸热反应 |
| C.a>b | D.a+1<b |