向某4L密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质浓度随时间变化如甲图所示。乙图为达到平衡后在t2、t3、t4、t5时改变某一种反应条件,平衡体系中速率随时间变化的情况,且所改变的条件均不同。已知t3-t4阶段为使用催化剂。则下列说法不正确的是:
A.若t1=15s,则t0—t1阶段以A浓度变化表示的反应速率v(A)为0.006mol/(L·s)
B.B的起始物质的量为0.08mol
C.若t2—t3阶段改变的条件是增大A的浓度,则平衡时C的体积分数变大
D.该反应为放热反应
能在水溶液中大量共存的一组离子是
| A.H+、I―、NO3―、SiO32- |
| B.Ag+、Fe3+、Cl―、SO42― |
| C.K+、SO42-、Cu2+、NO3― |
| D.NH4+、OH-、Cl-、HCO3- |
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是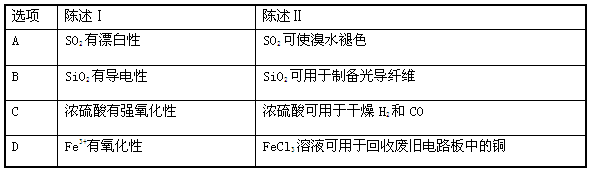
下列应用不涉及氧化还原反应的是
| A.Na2O2用作呼吸面具的供氧剂 |
| B.工业上电解熔融状态的Al2O3制备Al |
| C.工业上利用合成氨实现人工固氮 |
| D.实验室用NH4Cl和Ca(OH)2制备NH3 |
下列做法不正确的是
| A.易燃试剂与强氧化性试剂分开放置并远离火源 |
| B.用湿润的红色石蕊试纸检验氨气 |
| C.在50 mL量筒中配制0.100 0 mol·L-1碳酸钠溶液 |
| D.金属钠着火时,用细沙覆盖灭火 |
下列物质与水作用形成的溶液能与NH4Cl反应生成NH3的是
| A.二氧化氮 | B.钠 | C.硫酸镁 | D.二氧化硅 |