已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol/L的一元酸HA与b mol/L一元碱BOH等体积混合,可判定该溶液呈中性的依据是
| A.混合溶液的pH=7 |
B.混合溶液中,c(H+)=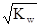 mol/L mol/L |
| C.a=b |
| D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-) |
下列化学反应的离子方程式不正确的是()
| A.铁屑溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |
| B.Fe(OH)3溶于过量的HI溶液:2Fe(OH)3+6H++2I━=2Fe2++I2+6H2O |
| C.在AlCl3溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| D.过量的NaHSO4溶液与Ba(OH)2溶液反应:2H++SO42━+Ba2++2OH━=BaSO4↓+2H2O |
下述实验设计能够达到目的的是()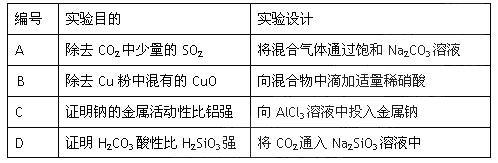
下列各组单质中,前者能将后者从化合物中置换出来的是()
①Al、Fe②C、Si③Mg、C④H2、Cu
A.只有①③ B.只有②④ C.①②③④ D.只有①②④
下列实验中金属或金属氧化物可以完全溶解的是()
| A.1 mol铜片与含2 mol H2SO4的浓硫酸共热 |
| B.常温下1 mol铝片投入足量的浓硫酸中 |
| C.1 mol MnO2粉末与含2 mol H2O2的溶液共热 |
| D.常温下1 mol铜片投入含4 mol HNO3的浓硝酸中 |
某同学通过系列实验探究Mg及其化合物的性质,操作正确且能达到目的的是()
| A.将水加入浓硫酸中得到稀硫酸,置镁条于其中探究Mg的活泼性 |
| B.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 |
| C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| D.将Mg(OH)2沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体 |