食盐、纯碱、食醋均为厨房中常用的物质,利用这些物质不能实现的实验是
①除去热水瓶内壁的水垢 ②检验自来水中是否含有氯离子
③检验镁粉中是否含有铝粉 ④鉴别食盐和纯碱
| A.①③ | B.②③ | C.②④ | D.①② |
钛(22Ti)金属常被称为未来钢铁。钛有46Ti、47Ti、48Ti、49Ti、50Ti等同位素,下列关于金属钛的叙述中不正确的是()
| A.上述钛原子中,中子数不可能为22 | B.钛元素在周期表中处于第四周期 |
| C.钛的不同同位素在周期表中处于不同的位置 | D.钛元素属于d区的过渡元素 |
A原子的结构示意图为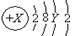 。则X、Y及该原子3p能级上的电子数分别可能为
。则X、Y及该原子3p能级上的电子数分别可能为
| A.18、6、4 | B.24、12、6 | C.18、8、6 | D.26、14、6 |
某元素质量数51,中子数28,其基态原子未成对电子数为
| A.0 | B.1 | C.2 | D.3 |
三氯化氮(NCl3)是一种淡黄色的油状液体,测得其分子具有三角锥形结构,则下面对于NCl3的描述不正确的是
| A.N原子是sp3杂化 | B.该分子中的氮原子上有孤对电子 |
| C.它还可以再以配位键与Cl-结合 | D.已知NBr3对光敏感,所以NCl3对光也敏感 |
下列有关σ键和π键的说法错误的是
| A.在某些分子中,化学键可能只有π键而没有σ键 |
| B.当原子形成分子时,首先形成σ键,可能形成π键 |
| C.一般情况下,同一个分子中的σ键比π键更稳定些 |
| D.含有π键的分子在反应时,π键是化学反应的积极参与者 |