常温下,Ksp(CaSO4)=9×l0-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图。下列判断错误的是
| A.a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液 |
| B.a点对应的Ksp等于c点对应的Ksp |
| C.向d点溶液中加入适量CaCl2固体可以变到c点 |
| D.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×l0-3mol/L |
提纯下列物质(括号内为少量杂质),所选用的除杂试剂与分离方法正确的是
| 不纯物质 |
除杂试剂 |
分离方法 |
|
| A |
乙酸乙酯(乙酸) |
饱和碳酸钠溶液 |
过滤 |
| B |
乙烷(乙烯) |
酸性高锰酸钾溶液 |
洗气 |
| C |
苯(Br2) |
KOH溶液 |
分液 |
| D |
苯(苯酚) |
浓溴水 |
过滤 |
有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为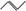 ,有机物X的键线式为
,有机物X的键线式为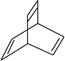
下列说法不正确的是
| A.X的化学式为C8H8 |
| B.X能使酸性高锰酸钾溶液褪色 |
| C.X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有4种 |
D.Y是X的同分异构体,且属于芳香烃,则Y的结构简式可以为 |
下列关于有机物叙述不正确的是
| A.甲烷、甲苯、乙醇、乙酸都可以发生取代反应 |
| B.煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏制取 |
| C.蔗糖可以水解生成葡萄糖和果糖 |
| D.植物油通过加氢可以变为脂肪 |
下列说法正确的是
A.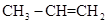 分子中所有原子一定处于同一平面 分子中所有原子一定处于同一平面 |
| B.除去乙烷中的乙烯是将混气通入酸性KMnO4溶液中 |
| C.若烃中碳、氢元素的质量分数相同,它们可能是同系物 |
| D.某烷烃的命名为3,4,4一三甲基己烷 |
下列关于有机化合物的说法正确的是
| A.糖类、油脂和蛋白质均可发生水解反应 |
| B.C5H12O能被催化氧化为醛的同分异构体有四种 |
| C.聚乙炔、聚苯乙烯和苯分子均含有碳碳双键 |
| D.甲酸丙酯和乙醛可用银氨溶液加以区别 |