下列关于电离常数(K)的说法中正确的是
| A.电离常数(K)越小,表示弱电解质电离能力越弱 |
| B.电离常数(K)与温度无关 |
| C.不同浓度的同一弱电解质,其电离常数(K)不同 |
| D.多元弱酸各步电离常数相互关系为K1<K2<K3 |
下列文字表述与反应方程式对应且正确的是()
A.实验室用液溴和苯在催化剂作用下制溴苯: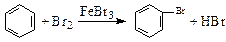 |
| B.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑ |
| C.钢铁的吸氧腐蚀正极反应:4OH- + 4e- ="=" O2↑+ 2H2O |
| D.+4价硫元素表现出还原性:H2SO3十2H2S==3S↓+3H2O |
下列叙述正确的是 ( )
| A.太阳能电池的主要材料是高纯度的二氧化硅 |
| B.C3N4和Si3N4结构相似,是新型的有机高温结构陶瓷 |
| C.Al2O3和Na2SiO3,都可作耐火材料 |
| D.工业上常用电解NaCl溶液来制备金属钠 |
下列有关金属的说法中,正确的是()
①纯铁不容易生锈②钠着火用水扑灭③铝在空气中耐腐蚀,所以铝是不活泼金属④缺钙会引起骨质疏松,缺铁会引起贫血⑤青铜、不锈钢、硬铝都是合金⑥ KSCN溶液可以检验Fe3+离子⑦ Al和Fe都能与某些氧化物反应
| A.①②⑤⑥ | B.②③④⑤ | C.①③④⑤⑦ | D.①④⑤⑥⑦ |
下列化学用语的表示中,不正确的是()
| A.NaHCO3电离方程式:NaHCO3 ="=" Na+ + HCO3- |
| B.苯的实验式:CH |
C.氢离子(H+)的结构示意图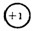 |
| D.甲酸乙酯的结构简式:HC-O-OC2H5 |
下列说法正确的是()
| A.刚刚结束的哥本哈根气候峰会,主题是低碳概念 |
| B.酸雨侵蚀建筑物,只发生了物理变化 |
| C.塑料袋、废纸等属于无机化合物 |
| D.生石灰遇水成为熟石灰,是CaO变成了CaCO3 |