NA表示阿伏加德罗常数,下列判断正确的是
| A.含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol/L |
| B.标准状况下,22.4 L空气含有NA个单质分子 |
| C.1 L 0.1 mol/L氨水含有0.1NA个OH- |
| D.在18 g 18O2中含有NA个氧原子 |
在25℃、101kPa 下:①2Na(s)+1/2O2(g)=Na2O(s)△H1=-414KJ/mol
②2Na(s)+O2(g)=Na2O2(s)△H2=-511KJ/mol
下列说法正确的是()
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s)△H=-317kJ/mol |
一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g) Z(g),60s达到平衡,生成0.3molZ,下列说法正确的是()
Z(g),60s达到平衡,生成0.3molZ,下列说法正确的是()
| A.以X浓度变化表示的反应速率为0.001mol/(L·s) |
B.将容器体积变为20L,Z的平衡浓度变为原来的 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的△H>0 |
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是()
①CO、O2②Cl2、CH4③NO2、O2④N2、H2
| A.①② | B.②④ | C.③④ | D.②③ |
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得: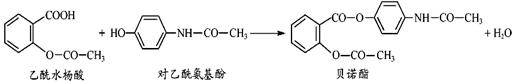
下列有关叙述正确的是()
| A.贝诺酯分子中有三种含氧官能团 |
| B.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚 |
| C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应 |
| D.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |
可用下图装置制取(必要时可加热)、净化、收集的气体是()
| A.铜和稀硝酸制一氧化氮 |
| B.亚硫酸钠与浓硫酸制二氧化硫 |
| C.锌和稀硫酸制氢气 |
| D.生石灰与浓氨水制氨气 |