下列反应的离子方程式正确的是
| A.实验室制二氧化碳:CaCO3 + 2H+ = Ca2++ CO2↑ + H2O |
| B.稀H2SO4与铁粉反应:2Fe + 6H+ = 2Fe3+ + 3H2↑ |
| C.氯气与水反应:Cl2 + H2O = Cl-+ ClO-+ 2H+ |
| D.AlCl3溶液与过量烧碱溶液反应:Al3+ + 3OH-=Al(OH)3↓ |
1993年的世界十大科技新闻称:中国学 者许志福和美国科学家穆尔共同合成了世界上最大的碳氢分子,其中1个分子由1134个碳原子和1146个氢原子构成。关于此物质,下列说法错误的是:
者许志福和美国科学家穆尔共同合成了世界上最大的碳氢分子,其中1个分子由1134个碳原子和1146个氢原子构成。关于此物质,下列说法错误的是:
| A.属于烃类 | B.常温下呈固态 |
| C.具有类似金刚石的硬度 | D.易被氧化 |
有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是:
A.分离、提纯→确定化学式→确定实验式→确定结构式
B.分离、提纯→确定实验式→确定化学式→确定结构式
C .分离、提纯→确定结构式→确定实验式→确定化学式
.分离、提纯→确定结构式→确定实验式→确定化学式
D.确定化学式→确定实验式→确定结构式→分离、提纯
下列推断或表述正确的是
A.在醋酸溶液的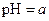 ,将此溶液稀释1倍后,溶液的 ,将此溶液稀释1倍后,溶液的 ,则 ,则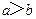 |
| B.向2.0mL浓度均为0.1 mol·L-1的KCl、KI混合液滴加1~2滴0.01 mol·L-1AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp小 |
| C.0.2 mol/L的一元酸HX与0.1 mol/L的KOH溶液等体积混合所得溶液中,一定有:c(H+)+ c(K+)= c(OH-)+ c(X-) |
| D.0.2 mol•L-1盐酸与等体积0.05 mol•L-1 Ba(OH)2溶液混合后,溶液pH为1 |
关于下列四个图像的说法中正确的是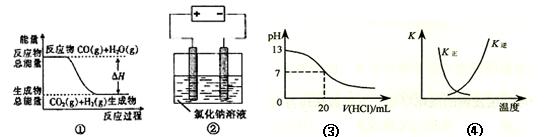
A.图①表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0 CO2(g)+H2(g)”中的△H大于0 |
| B.图②是在以石墨为电极电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1 |
| C.图③表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
D.图④中曲线表示反应2SO2(g) + O2(g)  2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化 |
将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+ 28HNO3 ==9Fe(NO3)x + NO↑+ 14H2O
下列判断合理的是
| A.Fe(NO3)x中的x为2 |
| B.反应中每还原0.4 mol氧化剂,就有1.2 mol电子转移 |
| C.稀HNO3在反应中只表现氧化性 |
| D.磁性氧化铁中的所有铁元素全部被氧化 |