研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为____________________________。利用反应6NO2+8NH3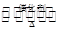 7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是________L。
7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是________L。
(2)已知:2SO2(g)+O2(g)  2SO3(g) ΔH="—196.6" kJ/mol ;
2SO3(g) ΔH="—196.6" kJ/mol ;
2NO(g)+O2(g)  2NO2(g) ΔH="—113.0" kJ/mol ;
2NO2(g) ΔH="—113.0" kJ/mol ;
①则反应NO2(g)+SO2(g)  SO3(g)+NO(g) 的ΔH=________ kJ/mol。
SO3(g)+NO(g) 的ΔH=________ kJ/mol。
②一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是___ _____。
| A.体系压强保持不变 |
| B.混合气体颜色保持不变 |
| C.SO3和NO的体积比保持不变 |
| D.每消耗1 mol SO3的同时生成1 mol NO2 |
③测得上述反应平衡时NO2与SO2的体积比为1∶6,则平衡常数K=__ _。
(3)催化剂存在下,NH3可用来消除NO的污染,生成两种对环境无害的物质。写出反应的化学方程式: ;该反应中氧化产物与还原产物的物质的量之比为 。
(4)氯碱工业的原料饱和食盐水中含有一定量的铵根离子,在电解时会生成性质极不稳定的三氯化氮,易引起爆炸。为除去饱和食盐水中的铵根离子,可在碱性条件下通入氯气,反应生成氮气。该反应的离子方程式为 。
(1)已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,
W的气态氢化物的稳定性比Y(填“强”、“弱”或“不一定”),W的原子序数(填“可能”或“不可能”)是Y的原子序数的2倍。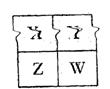
(2)已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层
电子数的一半,Y元素最高正价与它的负价代数和为6。M与其他物质的转化关系如下(部分产物已略去):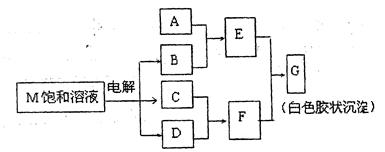
①若A是与X、Y同周期的一种常见金属,则A元素原子结构示意图为,
写出A与B溶液反应的离子方程式。
②若A是某元素的一种常见酸性氧化物,则该元素的周期表中的位置是,
写出E与F反应的化学方程式。
③电解M饱和溶液的产物之一B中的化学键为。工业上用电解物质M的另一产物氧化有毒含氰(CN-)碱性废水,得到无毒的N2、CO2等。写出此反应的离子反应方程式。
某有机化合物A的相对分子质量(分子量)大于110,小于 150。经分析得知,其中碳和氢的质量分数之和为52.24%,其
150。经分析得知,其中碳和氢的质量分数之和为52.24%,其 余为氧。请回答:
余为氧。请回答:
(1)该化合物分子中含有几个氧原子?为什么?
(2)该化合物的相对分子质量是。
(3)该化合物的化学 式是。
式是。
(4)该化合物分子中最多含个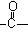 官能团。
官能团。
某温度下的wg只含C、H、O的有机物在足量氧气中充分燃烧。其燃烧产物立即与足量的过氧化钠反应。固体质量增加wg,试回答:
(1)符合此要求且相对分子质量最小的有机物A的结构式是_______ _________。
_________。
(2)符合此要求且相对分子质量是有机物A的2倍的有机物的结构简式是。
(3)符合此要 求的有机物的组成通式是___。
求的有机物的组成通式是___。
有机物A 是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂。
是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂。
(1)有机物A能够发生的反应有:(填写字母)
a.取代反应 b.加成反应 c.消去反应 d.酯化反应
(2)有机物A在Cu做催化剂和加热条件下,与氧气反应生成有机物B。B中的含氧官能团是:。
(3)有机物B经氧化后生成有机物C,C可有如下图所示的转化关系:
写出E的结构简式:;
(4)D在高温、高压和催化剂作用下反应生成HPMA,写出反应的化学方程式:
;
(5)F是E的一种同分异构体。0.1mol F与足量金属Na反应放出3.36L H2(标准状况下);0.1mol E与足量NaHCO3反应放出2.24L CO2(标准状况下);F能发生银镜反应。
F的结构简式可能是:_、。
2005年诺贝尔化学奖由法国科学家YvesChauvin、美国科学家RobertH.Grubbs、Richa rdR.Schrock共同获得。以表彰他
rdR.Schrock共同获得。以表彰他 们在烯烃复分解反应方面研究与应用所作出的贡献。已知烯烃的交叉复分解反应机理为双键断裂,换位连接。可表示为:
们在烯烃复分解反应方面研究与应用所作出的贡献。已知烯烃的交叉复分解反应机理为双键断裂,换位连接。可表示为:
又已知:R-CH2-CH=CH2+C12 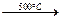 R-CHCl-CH=CH2+HCl。
R-CHCl-CH=CH2+HCl。
有机物R是烃的含氧衍生物(分子式为:C9H14O6),常用作纤维的增塑剂以及化妆品 等,F也可由油脂水解得到,有机物R的合成路线如下:
等,F也可由油脂水解得到,有机物R的合成路线如下: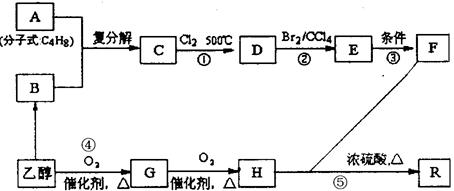
试回答下列问题
(1)写出反应①②的类型:①________________、②____________________;
反应③的反应条件______________________________________________
(2)写出结构简式,A:_____________________;E:____________________
(3)写出反应④⑤的化学方程式:
④_______________________________________________________
⑤_______________________________________________________