以下是对化学反应变化过程及结果的研究。按要求回答问题:
(1)已知:
甲醇脱水反应①2CH3OH(g)=CH3OCH3(g)+H2O(g) △H1=-23.9kJ·mol-1
甲醇制烯烃反应②2CH3OH(g)=C2H4 (g)+2H2O(g) △H2=-29.1kJ·mol-1
乙醇异构化反应③CH3CH2OH(g)=CH3OCH3(g)+H2O△H3=+50.7kJ·mol-1
则乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g)的△H= 。
(2)在25℃下,将pH=a的氢氧化钠溶液与pH=b的醋酸溶液等体积混合,若两溶液恰好完全反应,则a+b________14(填“>”、“<”或“=”);该温度下醋酸的电离常数K=__________(用含a、b的式子表示)。
(3)用一个离子方程式表示反应:100ml 3mol·L-1NaOH溶液中通入标准状况下4.48LCO2 ;所得溶液中离子浓度大小排列顺序为: ;
(4)废氨水可以转化成氨,氨再设计成碱性燃料电池。下图是该燃料电池示意图,产生的X气体可直接排放到大气中。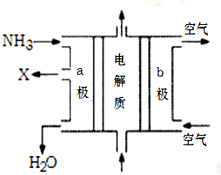
a电极电极反应式为 ;T℃下,某研究员测定NH3·H2O的电离常数为1.8×10-5,NH4+的水解平衡常数为1.5×10-8(水解平衡也是一种化学平衡,其平衡常数即水解常数),则该温度下水的离子积常数为 ,请判断T 25℃(填“>”“<”“=”)。
将蔗糖溶于水配成10%的溶液,分装在两支试管中。分别进行如下实验:
(1)在第一支试管中加入新制Cu(OH)2悬浊液并加热,没有红色沉淀产生,原因是____________________________;
(2)在第二个试管中加入几滴稀硫酸,再放在水浴中加热,再加入足量NaOH并加入新制Cu(OH)2悬浊液,加热。
①现象是__________________________;
②原因是__________________________;
③加入足量NaOH的作用是________________________;
④上述实验中发生的化学方程式是__________________。
油脂是重要的营养物质。某天然油脂A可发生下列反应: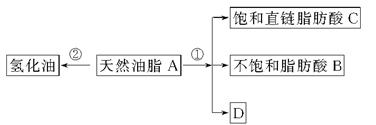
已知:A的分子式为C57H106O6。1 mol该天然油脂A经反应①可得到1 mol D、1 mol不饱和脂肪酸B和2 mol直链饱和脂肪酸C。经测定B的相对分子质量为280,原子个数比为C∶H∶O=9∶16∶1。
(1)写出B的分子式:________。
(2)写出反应①的反应类型:________;C的名称(或俗称)是________。
(3)近日,电视媒体关于“氢化油危害堪比杀虫剂”的报道引发轩然大波,反应②为天然油脂的氢化过程。下列有关说法不正确的是________。
a.氢化油又称人造奶油,通常又叫硬化油
b.植物油经过氢化处理后会产生副产品反式脂肪酸甘油酯,摄入过多的氢化油,容易堵塞血管而导致心脑血管疾病
c.氢化油的制备原理是在加热植物油时,加入金属催化剂,通入氢气,使液态油脂变为半固态或固态油脂
d.油脂的氢化与油脂的皂化都属于加成反应。
(4)D和足量金属钠反应的化学方程式:_________________________。
如图为硬脂酸甘油酯在碱性条件下水解的装置图,进行皂化反应时的步骤如下:
(1)在圆底烧瓶中加入7~8 g硬脂酸甘油酯,然后加入2~3 g的氢氧化钠、5 mL水和10 mL酒精,加入酒精的作用是________________________________。
(2)隔着石棉网给反应混合物加热约10 min,皂化反应基本完成,所得的混合物为________(填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入________,静置一段时间后,溶液分为上下两层,肥皂在________层,这个操作称为________。
(4)图中长玻璃导管的作用为__________________________________。
(5)写出该反应的化学方程式:________________________________。
一种有机物的结构简式为:
试回答下列问题:
(1)该化合物的种类是________。
A.烯烃 B.酯 C.油脂 D.高分子化合物
(2)该化合物的密度________。
A.比水大 B.比水小
(3)该化合物常温下的状态为________。
A.液体 B.固体 C.气体
(4)与该物质能反应的有________。
A.NaOH溶液 B.碘水
C.乙醇 D.乙酸 E.H2
写出该有机物与选出的化合物反应的化学方程式(任写一个):________。
对羟基苯甲酸丁酯(俗称尼泊金丁酯)可用作防腐剂,对酵母菌和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得。以下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
已知以下信息:
①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基;
②D可与银氨溶液反应生成银镜;
③F的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为1∶1。
回答下列问题:
(1)A的化学名称为________;
(2)由B生成C的化学反应方程式为________,该反应的类型为________;
(3)D的结构简式为________;
(4)F的分子式为________;
(5)G的结构简式为________;
(6)E的同分异构体中含有苯环且能发生银镜反应的共有________种,其中核磁共振氢谱有三种不同化学环境的氢,且峰面积比为2∶2∶1的是________(写结构简式)。