(10分)化学是一门以实验为基础的学科,试回答以下问题。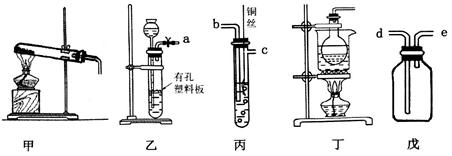
(1)实验室中制取并收集少量氨气,可选用上述____________(填装置序号)装置,氨气应从收集装置的____________(填字母序号)导管进气。
(2)选用装置乙、丙、戊制备、收集一氧化氮气体,乙中塑料板上若放置石灰石,戊中盛满稀NaOH溶液,正确的连接顺序为___________________(用接口字母表示),装置乙的作用是____________,丙中产生NO的离子方程式为____________________________。
(3)二氧化氯(C1O2)是一种常用高效消毒剂,某研究小组利用丁装置制备C1O2。
①在烧瓶中放入KClO3和草酸(H2C2O4),然后加入足量的稀硫酸,水浴加热。反应生成ClO2、CO2和K2SO4,则该反应中氧化产物与还原产物物质的量之比为_________;
②温度过高时,二氧化氯的水溶液有可能发生爆炸。在反应开始前将烧杯中的水加热到80%,然后停止加热,并使其保持在60℃~80℃之间,丁装置中缺少的一种必需的玻璃仪器名称是_______________;
③将二氧化氯溶液加入到硫化氢溶液中,然后加入少量的稀盐酸酸化过的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式________________。
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: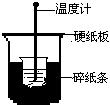
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________。
(2)大烧杯上如不盖硬 纸板,求得的中和热数值将_______(填“偏大”、“偏小”或“无影响”)。
纸板,求得的中和热数值将_______(填“偏大”、“偏小”或“无影响”)。
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量________(填“相等”或“不相等”),但中和热应_________(填“相等”或“不相等”),简述理由_________________________________。
《硫酸铜晶体里结晶水含量的测定》是中学化学中的重要实验,请回答下列该实验的相关问题。
(1)实验中能直接加热的仪器名称为____________;进行的称量操作至少为________次。
(2)下列操作会引起测定结果偏高的是__________________
| A.加热时温度过高CuSO4发生分解 | B.加热后在空气中冷却再称量 |
| C.加热过程中有晶体溅出 | D.晶体部分风化 |
二氯化二硫(S2C12)在工业上用于橡胶的硫化。为了在实验室合成S2C12,某化学研究性学习小组查阅了有关资料,得到如下信息:
①在110℃~ 140℃时,将干燥的氯气与硫反应可得到S2C12的粗产品。 ②有关物质的部分性质如下表:
②有关物质的部分性质如下表:
| 物质 |
熔点/℃ |
沸点/℃ |
化学性质 |
| S |
112.8 |
444.6 |
略 |
| S2C12 |
-77 |
137 |
S2C12遇水生成HCl、SO2、S,300℃以上完全分解; S2C12 + C12 2SCl2 2SCl2 |
| SCl2 |
-121 |
59.6(分解) |
设计实验装置如下图: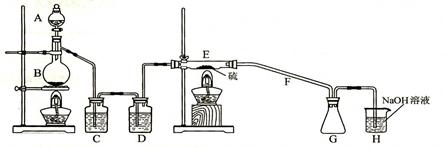
(1)仪器A,B的名称分别为______________,______________。
A中发生反应的离子方程式为。
C中的试剂名称是______________;仪器D的作用是。
(2)上图中装置不够完善,请你提出改进意见;
利用改进后的正确装置进行实验,请回答下列问题:
(3)E中反应的化学方程式为_____________________________________________。
(4)如果在加热E时温度过高,对实验结果的影响是_________________________,
在F中可能出现的现象是_________________________________________。
(5)S2C12粗品中可能混有的杂质是、、___________,为了提高S2C12的纯度,关键的操作是控制好温度和______________________。
实验题:现有药品:W g(W<1)锌片、稀硫酸、无水硫酸铜、氧化铜和水。请从图中选用适当的实验装置,设计一个简单的实验,粗略测定锌的相对原子质量(假设环境为标准状况)。
(1)应选用的装置是(只要求写出图中装置的标号)。
(2)所用装置的连接顺序是(填各接口的字母,胶管省略)。
(3)为了保证不漏出氢气,操作中加放试剂 的方法是。
的方法是。
(4)用实验所测得的数据,写出计算锌的相对原子质量的数学式:Mr(Zn)=。
(8分)现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:
 ①2Mg+O2
①2Mg+O2 2MgO;
2MgO;
②3Mg+N2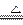 Mg3N2;
Mg3N2;
③2Mg+CO2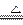 2MgO+C;
2MgO+C; ④Mg+H2O
④Mg+H2O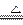 MgO+H2↑;
MgO+H2↑;
⑤Mg3N2 +6H2O =3Mg(OH)2↓+2NH3↑
 可供选择的装置和药品如上图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。
可供选择的装置和药品如上图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。 回答下列问题
回答下列问题



 (1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)。
(1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)。 (2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)。
(2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)。 (3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响?
(3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响?
,原因是。 (4)请设计一个实验,验证产物是氮化镁:。
(4)请设计一个实验,验证产物是氮化镁:。