丙酮(CH3COCH3)在某溶剂里,在催化剂作用下发生反应: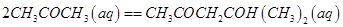 取相同浓度的
取相同浓度的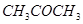 ,分别在40℃和60℃时,测得其转化率
,分别在40℃和60℃时,测得其转化率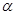 随时间变化的关系曲线(
随时间变化的关系曲线(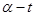 )如图所示。下列说法正确的是
)如图所示。下列说法正确的是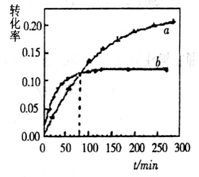
A.b代表40℃时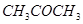 的 的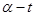 曲线 曲线 |
| B.升高温度可缩短该反应达平衡的时间并能提高平衡转化率 |
| C.增大压强可缩短该反应达平衡的时间并能提高平衡转化率 |
| D.上述反应的逆反应为吸热反应 |
如图所示是101kPa时,氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是()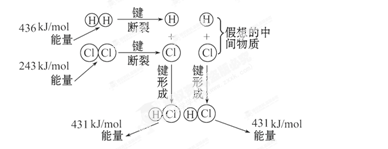
| A.此反应的热化学方程式为:H2(g)+Cl2(g) =2HCl(g) ΔH=+183kJ·mol-1 |
| B.2molHCl分子中的化学键形成时要释放862kJ能量 |
| C.1molH2中的化学键断裂时需要吸收436kJ能量 |
| D.此反应的热化学方程式为:1/2H2(g)+1/2Cl2(g) =HCl(g) ΔH=-91.5kJ·mol-1 |
在下列各说法中,正确的是()
A.对于2SO2(g)+O2(g)  2SO3(g) ΔH=-QkJ·mol-1,(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2 kJ 2SO3(g) ΔH=-QkJ·mol-1,(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2 kJ |
| B.热化学方程式中的化学计量数不能用分数表示 |
| C.Zn(s)+H2SO4(aq) =ZnSO4(aq)+H2(g) ΔH<0,该反应的化学能可以转化为电能 |
| D.ΔH的大小与热化学方程式的化学计量数无关 |
在一定条件下,A和B反应可生成C和D,其能量变化如下:
下列有关反应A+B=C+D的说法正确的是()
| A.反应前后原子的种类和数目可能改变 |
| B.该反应若有热量变化,则一定是氧化还原反应 |
| C.若该反应为放热反应,则不需加热反应就一定能进行 |
| D.该反应遵循能量守恒,所以一定有能量变化 |
下列反应既是氧化还原反应,又是吸热反应的是()
| A.实验室制备氢气 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.灼热的碳与水的反应 | D.铝粉与氧化铁粉末反应 |
下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是()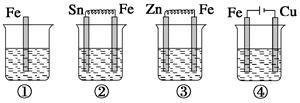
| A.②>①>③>④ | B.④>②>①>③ |
| C.④>②>③>① | D.③>②>④>① |