乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是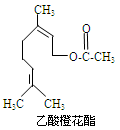
①分子式为C12H20O2 ②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属于芳香族的化合物
的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol
| A.①②③ | B.①②⑤ | C.①②⑤⑥ | D.①②④⑤⑥ |
常温时,0.1mol/LHA溶液的pH>1,0.1mol/L BOH溶液中c(OH-): c(H+)=1012,将这两种溶液等体积混合,以下离子浓度关系判断正确的是()
| A.c(H+)<c(OH-)=c(A-)<c(B+) |
| B.c(OH-)<c(H+)<c(B+)<c(A-) |
| C.c(H+)<c(OH-)<c(A-)<c(B+) |
| D.c(A-)= c(B+)>c(H+)=c(OH-) |
铅蓄电池是一种典型的可充电电池,电池总反应式为Pb+PbO2+4H++2
 2PbSO4+2H2O,则下列说法正确的是( )
2PbSO4+2H2O,则下列说法正确的是( ) 
| A.放电时,电流方向由B过M到A |
| B.充电时,铅蓄电池的正极应与充电器电源的负极相连 |
C.放电时,正极反应是Pb-2e-+ ====PbSO4 ====PbSO4 |
D.充电时,阳极反应是PbSO4-2e-+2H2O====PbO2+ +4H+ +4H+ |
25℃时,下列各溶液中有关物质的量浓度关系正确的是()
| A.c(NH+4)相等的(NH4)2CO3溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2CO3]<c(NH4Cl) |
| B.Na2CO3溶液中:2c(Na+)=c(CO2-3)+c(HCO-3)+c(H2CO3) |
| C.NH4HSO4溶液中滴加NaOH至溶液恰好呈中性: c(Na+)>c(SO2-4)>c(OH-)=c(H+) |
| D.pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合: |
c(Na+)>c(CH3COO)>C(OH-)>c(H+)
在密团容器中充入1molCO和1molH2O(气),在一定条件下达到平衡时生成了2/3mol CO2(反应为CO+H2O(g)  CO2+H2),当其他条件不变,充入的水蒸气改变为2mol时,平衡时生成CO2的物质的量可能是()
CO2+H2),当其他条件不变,充入的水蒸气改变为2mol时,平衡时生成CO2的物质的量可能是()
| A.2/3mol | B.3/4mol | C.4/5mol | D.1mol |
下列离子方程式中正确的是()
| A.向Ba(OH)2溶液逐滴加入NH4HSO4溶液至刚好沉淀完全: Ba2++OH-+H++SO  =BaSO4↓+H2O =BaSO4↓+H2O |
B.用Pt电极电解MgCl2溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
C.碳酸氢钠溶液与硫酸溶液反应:HCO +H+=CO2↑+H2O +H+=CO2↑+H2O |
| D.将少量氨水滴入硝酸银溶液中:Ag++2NH3·H2O=[Ag(NH3)2]++2H2O |