聚乳酸的结构为 有机物的相关叙述正确的是
有机物的相关叙述正确的是
| A.其单体不能发生消去反应 |
| B.其单体可以通过反应形成六元环状化合物 |
C.其单体含有 |
| D.聚乳酸是由加聚反应获得 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,11.2 L乙醇所含的羟基数为0.5NA |
| B.常温下,1L 0.1 mol·L-1的Na2CO3溶液中含有的离子总数为0.3NA |
| C.常温常压下,5.6g乙烯和环丙烷的混合气体中含有的碳原子数为0.4NA |
| D.电解硫酸铜溶液时,阳极每生成标准状况下3.36L气体,电路中转移电子数为0.3NA |
下列有关化学用语使用正确的是
A.CO2的电子式: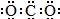 |
B.核内有8个中子的碳原子: 8 6C |
C.钾原子结构示意图: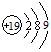 |
D.乙烯的比例模型: |
2010年诺贝尔化学奖授予“钯催化交叉偶联反应”的研究,采用钯催化可将碳原子连接在一起制造新的有机材料。下列说法不正确的是
| A.钯催化剂能提高碳原子反应的活性 |
| B.钯催化剂能催化所有类型的有机反应 |
| C.“钯催化交叉偶联反应”有利于人类合成复杂分子 |
| D.利用该技术能改变合成路径,降低反应发生的条件 |
用惰性电极电解一定量的硫酸铜溶液,实验装置如图①。电解过程中的实验数据如图②,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。则下列说法正确的是()
| A.电解过程中,b电极表面先有红色物质析出,后有气泡产牛 |
| B.a电极上发生的反应方程式为:2H++2e-一H2↑和4OH-—4e-==2H2O十O2↑ |
| C.曲线0~P段表示H2和O2混合气体的体积变化,曲线P~Q段表示O2的体积变化 |
| D.从开始到Q点时收集到的混合气体的平均摩尔质量为17g·mol-1 |
一定温度下,lmol X和n mol Y在锌积为2L的密闭容器中发生如下反应:
X(g)+Y(g) 2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是()
2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是()
| A.用X表示此反应的反应速率是(0.1—0.2a)mol·(L·min)-1 |
B.向l平衡后的体系中加入lmol M,平衡向逆反应 方向移动 方向移动 |
| C.当混合气体的质量不再发生变化时,说明反应达到平衡状态 |
| D.向上述平衡体系中再充入lmol X,v(正)增大,v(逆)减小,平衡正向移动 |