用质量均为100 g的铜作电极,电解硝酸银溶液,电解一段时间后,两电极的质量差为28 g,此时两电极的质量分别为
| A.阳极100 g,阴极128 g | B.阳极91.0 g,阴极119.0 g |
| C.阳极93.6 g,阴极121.6 g | D.阳极86.0 g,阴极114.0 g |
NA代表阿伏加德罗常数的值。下列叙述正确的是
| A.60 g丙醇中存在的共价键总数为10 NA |
| B.50 mL 18.4 mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| C.钠在空气中燃烧可生成多种氧化物。23 g钠充分燃烧时转移电子数为1 NA |
D.235 g核素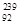 U发生裂变反应: U发生裂变反应: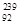 U + U + 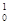 n n 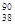 Sr + Sr + 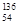 U + 10 U + 10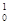 n净产生的中子( n净产生的中子(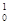 n)数为10 NA n)数为10 NA |
分类是化学学习与研究的常用方法,下列分类正确的是
| A.Na2O、MgO、Al2O3均属于碱性氧化物 |
| B.石灰石、生石灰、熟石灰均属于碱 |
| C.酸、碱、盐之间发生的反应均属于复分解反应 |
D.混合物、分散系、胶体从属关系如图所示 |
已知:将一定量Cl2通入KOH溶液,可能生成KCl、KClO、KClO3,且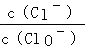 的值与温度高低有关.当n(KOH)="6a" mol时,下列有关说法错误的是
的值与温度高低有关.当n(KOH)="6a" mol时,下列有关说法错误的是
A.若某温度下,反应后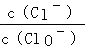 =11,则溶液中 =11,则溶液中 =0.5 =0.5 |
| B.参加反应的氯气的物质的量等于3a mol |
| C.改变温度,反应中转移电子的物质的量ne的范围:3a mol<ne<5a mol |
| D.改变温度,产物中KClO3的最大理论产量为2a mol |
只用下表提供的仪器、试剂,就能达到相应实验目的的是
| 选项 |
仪器 |
试剂 |
相应实验目的 |
| A |
托盘天平(带砝码)、滴管、量筒、烧杯、药匙、玻璃棒 |
食盐,蒸馏水 |
配制500ml一定物质的量浓度的NaCl溶液 |
| B |
烧杯、漏斗、滴管、铁架台(带铁圈)、玻璃棒、滤纸、导气管 |
AlCl3溶液(含少量MgCl2),烧碱,CO2,稀盐酸 |
除去AlCl3溶液中少量的MgCl2 |
| C |
铁架台(带铁圈、铁夹)、分液漏斗、洗气瓶、烧杯、圆底烧瓶、导管(若干)、石棉网 |
MnO2、稀盐酸、浓硫酸、饱和食盐水、氢氧化钠溶液 |
制备干燥纯净的Cl2 |
| D |
分液漏斗、烧瓶、锥形瓶、导管、橡皮塞 |
稀盐酸,大理石,硅酸钠溶液 |
证明非金属性:Cl>C>Si |
一种瑞香素的衍生物的结构简式如图,下列有关该有机物性质的说法正确的是
| A.能与FeCl3溶液发生显色反应 |
| B.1mol该有机物最多可与3molH2加成 |
| C.1mol该有机物最多可与含5molNaOH的溶液反应 |
| D.1mol该有机物与足量NaHCO3溶液反应可放出3molCO2 |