金属及其化合物转化关系是化学学习的重要内容之一。下列各组物质的转化关系,不全部是通过一步反应完成的是
| A.Na→NaOH→Na2CO3→NaCl | B.Al→Al2O3→Al(OH)3→AlCl3 |
| C.Mg→MgCl2→Mg(OH)2→MgSO4 | D.Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
2011年3月11日日本发生9级地震,福岛核电站发生核泄漏,主要放射性物质为131 53I,下列有关131 53I叙述错误的是
| A.131 53I是碘的一种核素 |
| B.131 53I是一种新发现的元素 |
| C.131 53I质量数为131 |
| D.131 53I核内的中子数与核外电子数之差为25 |
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列不属于未来新能源标准的是
①天然气②煤③氢能④石油⑤太阳能⑥生物质能⑦风能
| A.①②④ | B.⑤⑥⑦ |
| C.③⑤⑥ | D.③⑤⑦ |
“绿色食品”和“白色污染”是指
| A.绿颜色的食品和白色建筑物 |
| B.有叶绿素的食品和水泥厂排放的白色粉尘 |
| C.安全无公害的营养食品和聚乙烯等白色塑料垃圾 |
| D.经济附加值高的营养食品和治炼厂的白色烟尘 |
按下图装置,持续通入X气体,可以看到a处有红棕色物质生成,b处变蓝,c处得到液体,则X气体是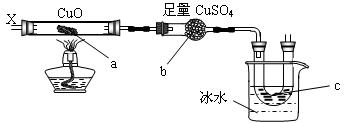
| A.H2 | B.CO和H2 | C.CO2 | D.CH3CH2OH(气) |
下列物质中既属于有机物,又属于酸的是
| A.H2CO3 | B.CH3OH | C.CH3CH2OH | D.CH3COOH |