工业制硝酸经以下一系列反应: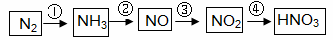
请回答:
(1)写出反应④的化学方程式 ,实验室收集NO的方法是 。
(2)对于氮的化合物,下列说法不正确的是(选填序号字母) 。
a.氨可用作制冷剂
b.铵态氮肥一般不能与碱性化肥共同使用
c.硝酸可用于制化肥、农药、炸药、染料、盐类等
d.某浓硝酸中含有溶质2mol,标准状况下,该浓硝酸与足量的铜完全反应能生成1mol NO2
(3)已知:H2(g)+1/2 O2(g)=H2O(g) △H1=-241.8kJ/mol
N2(g)+ 3H2(g)=2NH3(g) △H2=-92.0kJ/mol
则34g氨气与氧气反应生成N2(g)与H2O(g)时,△H= kJ/mol。
(4)氨气在微生物的作用下与氧气反应生成HNO2,写出该反应的化学方程式 。
(5)氨气是氮肥工业的重要原料,某化肥厂生产铵态氮肥(NH4)2SO4的部分工艺流程如下: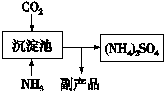
向装有CaSO4悬浊液的沉淀池中先通氨气,再通CO2的原因(请从溶解度和溶解平衡角度分析) 。
在密闭容器中进行的反应C(s)+ H2O(g)  CO(g) + H2(g)
CO(g) + H2(g)  ,改变下列条件:(1)若升高温度,正反应速率,逆反应速率(填增大或减小或不变),平衡移动。
,改变下列条件:(1)若升高温度,正反应速率,逆反应速率(填增大或减小或不变),平衡移动。
(2)若增大CO的浓度,平衡移动,H2O(g)的转化率(填增大或减小或不变)。
在200ml 0.5 mol·L-1的Al2(SO4)3溶液中,Al3+的物质的量浓度是,Al3+的质量是,SO42-的个数是。
(4分) 0.1mol某气体的质量为6g ,该气体的摩尔质量为,该气体在标况下的体积为。
(4分)在同温同压下,两个体积相同的玻璃容器中分别盛满O3和O2 ,容器中的O3和O2的质量之比为,密度之比为。
9g水的物质的量是mol,含个氧原子,mol氢原子。