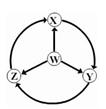
如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是
| 选项 |
W |
X |
Y |
Z |
 |
| A |
S |
SO2 |
SO3 |
H2SO4 |
|
| B |
Na |
Na2O2 |
NaOH |
NaCl |
|
| C |
Fe |
FeCl3 |
Fe(OH)2 |
FeCl2 |
|
| D |
Al |
AlCl3 |
NaAlO2 |
Al2(SO4)3 |
已知Ksp(AgCl)=1.8×10—10,Ksp(AgI)=1.5×10—16,Ksp(AgBr)=7.7×10—13,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
| A.AgCl>AgI> AgBr | B.AgCl> AgBr>AgI |
| C.AgBr >AgCl>AgI | D.AgBr >AgI>AgCl |
a、b、c、d是HCl、BaCl2、AgNO3、Na2CO3四种溶液中的一种,现将它们两两混合,现象如下表所示:由上述现象可推知a、b、c、d依次是
| 反应物 |
a+b |
c+d |
a+d |
a+c |
b+d |
| 现象 |
白色沉淀 |
白色沉淀 |
白色沉淀 |
白色沉淀 |
无色气体 |
A.HCl、BaCl2、AgNO3、Na2CO3
B.AgNO3、HCl、BaCl2、Na2CO3
C.AgNO3、HCl、Na2CO3、BaCl2
D.BaCl2、Na2CO3、AgNO3、HCl
将K2SO4、Al2(SO4)3两种盐混合于硫酸酸化的水中,测得c(SO42-)=0.03 mol/L,c(Al3+)=0.005 mol/L,c(H+)=0.01 mol/L(假设溶液中H2SO4完全电离为H+和SO42-),则c(K+)为
| A.0.045 mol/L | B.0.035 mol/L |
| C.0.005 mol/L | D.0.040 mol/L |
下列从混合物中分离出其中的一种成分,所采取分离方法正确的是
| A.利用碘单质在酒精中的溶解度大,用酒精把碘水中的碘单质萃取出来 |
| B.要分离汽油和水,最好使用蒸馏法 |
| C.从含有少量氯化钠的硝酸钾溶液中提取硝酸钾,可以利用溶解度随温度变化的差异采取结晶法 |
| D.要从在实验室加热氯酸钾和二氧化锰的混合物中分离得到二氧化锰,应使用分液漏斗进行分离 |
现有NaOH、Na2CO3和Ba(OH)2三种无色溶液,用一种试剂就可将它们鉴别出来,这种试剂是
| A.HCl | B.H2SO4 | C.Na2SO4 | D.CaCl2 |