下列A-D各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
| |
甲 |
乙 |
丙 |
| A |
Al2O3 |
HNO3 |
Ba(OH)2 |
| B |
NH3 |
O2 |
H2SO4 |
| C |
SiO2 |
NaOH |
HF |
| D |
CO2 |
Na2O2 |
H2O |
钛被称为“第三金属”,其制取原料为金红石(TiO2),制取步骤为:
TiO2→TiCl4 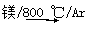 Ti
Ti
已知:①C(s)+O2(g)=CO2(g) ,ΔH1
②2CO(g)+O2(g)=2CO2(g) ,ΔH2
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ,ΔH3
则反应TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH为
| A.ΔH3+2ΔH1+2ΔH2 | B.ΔH3+2ΔH1+ΔH2 |
| C.ΔH3+2ΔH1-ΔH2 | D.ΔH3+2ΔH1-2ΔH2 |
合成氨的反应是:N2(g)+3H2(g) 2NH3(g);△H<0。使产率增大的方法是
2NH3(g);△H<0。使产率增大的方法是
| A.升高温度 | B.降低压强 | C.使用催化剂 | D.及时分离出NH3 |
下列说法正确的是
| A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则1mol H2SO4和1mol Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)= 2CO(g)+O2(g)反应的△H=+(2×283.0)kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
下列事实,不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+ H2O  HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 |
B.对CO(g) + NO2 (g)  CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深 CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深 |
| C.升高温度能够增大硝酸钾在水中的溶解度 |
| D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施 |
同体积的pH=3的强酸溶液和弱酸溶液分别跟等质量的镁充分反应,下列错误的
| A.刚开始时两种溶液中产生H2的速率相同 |
| B.若有一种溶液中镁有剩余,则有剩余的是强酸溶液 |
| C.若两种溶液中镁均无剩余,则两者产生等量的氢气 |
| D.若两种溶液中镁均有剩余,则两者产生等量的氢气 |