(1)已知C(石墨,s)= C(金刚石,s);△H>0,则稳定性:金刚石 石墨(填>或<)
(2)已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2。则△H1 △H2(填>或<)
(3)“嫦娥五号”预计在海南文昌发射中心发射,火箭的第一、二级发动机中,所用的燃料为偏二甲肼和四氧化二氮,偏二甲肼可用肼来制备. 用肼(N2H4)为燃料,四氧化二氮做氧化剂,两者反应生成氮气和气态水.
已知:N2(g)+2O2(g)=N2O4(g) △H="+10.7kJ·" mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H="-543" kJ· mol-1
写出气态肼和N2O4反应的热化学方程式为 。
(4)25℃,101kPa时,14gCO在足量的O2中充分燃烧,放出141.3 kJ的热,则CO的燃烧热为△H= 。
(5)0.50L 2.00mol/L H2SO4溶液与2.10L 1.00mol/L KOH溶液完全反应,放出114.6kJ的热量,该反应的中和热为△H=
(6)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391 kJ、
946 kJ,则N2与H2反应生成NH3的热化学方程式是 。
(本题6分)
⑴电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
①检验溶液中Fe3+存在的试剂是 __,证明Fe3+存在的现象是 __。[来]②写出FeCl3溶液与金属铜发生反应的化学方程式:。
⑵ 3Cl2+ 6NaOH ="=" 5NaCl + NaClO3+ 3H2O
氧化剂与还原剂的物质的量之比为,氧化产物是 ________。
室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体。在合适反应条件下,它们可以按下面框图进行反应;E是无色溶液,F是淡绿色溶液。B和C反应发出苍白色火焰。请回答:(本题9分)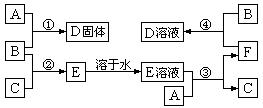
(1)A是__________,B是__________,C是__________(请填写化学式);
(2)反应①的化学方程式______________________________;
(3)反应③的离子方程式______________________________;
(4)反应④的离子方程式______________________________。
写出下列反应的化学方程式或离子方程式:(本题8分)
⑴氯化铁溶液中加入铁粉
化学方程式:____________________________________
⑵碳酸氢钠溶液滴入盐酸中
离子方程式:________________________________________
⑶碳酸氢钠溶液和氢氧化钠溶液反应
化学方程式:________________________________________
⑷将二氧化碳通入炽热的炭层
化学方程式:________________________________________
填写下列空格(本题3分)
| 化学反应方程式 |
氧化剂 |
还原剂 |
| Zn + 2HCl = ZnCl2 + H2↑ |
||
| 3NO2 + H2O= 2HNO3+ NO |
||
C+H2O(气)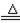 CO+H2 CO+H2 |
在CaCO3、CO2、CO、Na2CO3、NaHCO3、Cl2物质中(本题3分)
⑴大气中过多会造成温室效应的是_______________.
⑵俗名是小苏打,且是制糕点发酵粉的主要成分的是________
⑶能和血液中血红蛋白结合而使人中毒的是_________________
⑷是水垢的主要成分_______________
⑸能用于制造漂白粉的是__________________
⑹俗名是纯碱,工业上用于造纸业的是___________