下列陈述Ⅰ、Ⅱ错误或因果关系不成立的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
某吸热反应能自发进行 |
该反应是熵增反应 |
| B |
NH4F水溶液中含有HF |
NH4F溶液不能存放于玻璃试剂瓶中 |
| C |
常温下浓硫酸存放在铝制的器皿中 |
浓硫酸不与铝反应 |
| D |
氢氧化铝可作胃酸的中和剂 |
氢氧化铝是两性氢氧化物 |
在下列变化①工业制盐酸 ②工业制漂粉精 ③实验室制氯气中,按氯元素被氧化、被还原、既被氧化又被还原的顺序排列,正确的是
| A.①②③ | B.②①③ | C.①③② | D.③①② |
下列实验过程中,始终无明显现象的是
| A.NO2通入FeSO4溶液中 | B.CO2通入CaCl2溶液中 |
| C.NH3通入AlCl3溶液中 | D.SO2通入Ba(NO3)2溶液中 |
“酸化”是实验中经常采用的方法,下列酸化正确的是
| A.抑制Fe2+的水解,用稀硝酸酸化 |
| B.提高高锰酸钾的氧化能力,用盐酸酸化 |
| C.确认溶液中含有SO42—时,用盐酸酸化,再检验 |
| D.检验氯代烃中含氯 ,加碱溶液加热后,用硫酸酸化,再检验 |
下列物质在水中最难电离出氢离子的是
| A.CH3COOH | B.C2H5OH | C.H2O | D.C6H5OH |
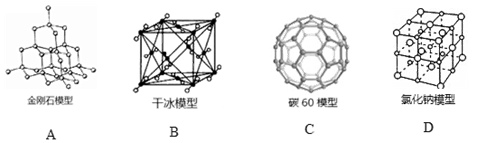
下列晶体模型对应的物质熔化时破坏共价键的是