常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1 mol·L-1氨水溶液:K+、Na+、NO3-、AlO2- |
| B.0.1 mol·L-1 Fe(NO3)2溶液:H+、Al3+、SO42-、Cl- |
| C.滴入酚酞显红色的溶液:Na+、Mg2+、NO3-、HCO3- |
| D.由水电离出的c(H+)=10-11mol·L-1的溶液:Ca2+、NH4+、Cl-、CO32- |
电解NO制备 NH4NO3的工作原理如图所示,X、Y皆Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A。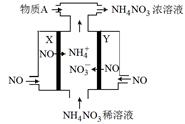
下列说法正确的是
A.物质A为NH3
B.X电极为电解池阳极
C.Y电极上发生了还原反应
D.Y电极反应式为NO-3e-+4OH-==NO+2H2O
25℃时,相同pH值的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH值随溶液体积变化的曲线如图所示。
下列说法正确的是
A.同浓度的NaA与NaB溶液中,c(A-) 小于c(B-)
B.a点溶液的导电性大于b点溶液
C.a点的c(HA)大于b点的c(HB)
D.HA 的酸性强于HB
为测定石灰石样品中碳酸钙(含SiO2杂质)的含量。现利用下图所示装置进行实验,充分反应后,测定装置C中生成的BaCO3沉淀质量。下列说法正确的是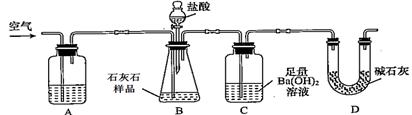
| A.装置A中药品应为浓硫酸 |
| B.在B—C之间应增添盛有饱和NaHCO3溶液的洗气装置,以除去氯化氢气体 |
| C.为了测得C中生成的沉淀质量,需经过过滤、洗涤、干燥、称量等操作 |
| D.只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数 |
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-中的几种。①用pH试纸测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是
| A.Na+ | B.SO42- | C.Ba2+ | D.NH4+ |
下列实验方案中,不能达到实验目的的是
| 选项 |
实验目的 |
实验方案 |
| A |
鉴别溴蒸气和NO2 |
分别通入硝酸银溶液中,产生淡黄色沉淀的是溴蒸汽 |
| B |
证明氧化性:H2O2比Fe3+强 |
用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
| C |
证明盐类水解是吸热反应 |
在醋酸钠溶液中滴入酚酞试液,加热后红色加深 |
| D |
证明难溶物存在沉淀溶解平衡 |
往黄色固体难溶物PbI2加水中振荡,静置取上层清液加入NaI固体产生黄色沉淀 |