某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化如图所示,下列说法正确的是
| A.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,Mg2++2OH-= Mg(OH)2↓ |
| B.原溶液中含有的阳离子必定有H+、NH4+、Al3+、Mg2+ |
| C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 |
| D.d点溶液中含有的溶质只有NaAlO2 |
对于化学反应的限度的叙述,错误的是
| A.任何可逆反应都有一定的限度 |
| B.化学反应的限度是不可改变的 |
| C.相同条件下,不同的可逆反应,其反应的限度不同 |
| D.化学反应达到限度时,正逆反应速率相等 |
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g) 2C(g)。若经2s 后测得C的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质A表示的反应的平均速率为 0.6 mol·(L·s)-1;② 用物质B表示的反应的平均速率为 0.15 mol·(L·s)-1;③ 2s 时物质A的浓度为1.4 mol·L-1;④2s 时物质B的转化率为70% 。其中正确的是
2C(g)。若经2s 后测得C的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质A表示的反应的平均速率为 0.6 mol·(L·s)-1;② 用物质B表示的反应的平均速率为 0.15 mol·(L·s)-1;③ 2s 时物质A的浓度为1.4 mol·L-1;④2s 时物质B的转化率为70% 。其中正确的是
| A.①③ | B.①④ | C.②③ | D.③④ |
有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B为正极。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是
A. D A B C B.D C A B C. B A D C D.A B C D
已知:2SO2+O2 2SO3为放热反应,对该反应的下列说法中正确的是
2SO3为放热反应,对该反应的下列说法中正确的是
| A.SO2的能量一定高于SO3的能量 | B.因该反应为放热反应,故不必加热就可发生 |
| C.O2的能量一定高于SO2的能量 | D.SO2和O2的总能量一定高于SO3的总能量 |
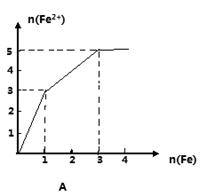
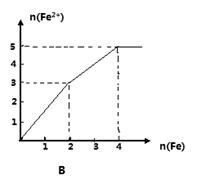
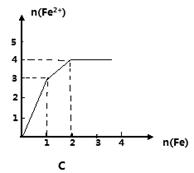
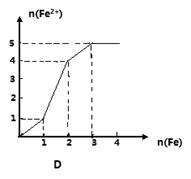
某稀溶液中含有等物质的量的ZnSO4, Fe2(SO4)3, H2 SO4, CuSO4,向其中逐渐加入铁粉,溶液中Fe2+的物质的量(纵坐标/mol)和加入铁粉的物质的量(横坐标/mol)之间的关系为()