(12分) 金属冶炼和处理常涉及许多反应。
(1)由下列物质冶炼相应金属时采用电解法的是______
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应2Cu2S + 2H2SO4 + 5O2 = 4CuSO4 + 2H2O,
该反应的还原剂是______,当1molO2发生反应时,还原剂所失电子的物质的量为______mol。
(3)下图为电解精炼银的示意图,______(填a或b)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为 。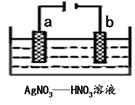
(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为 ,其总反应式为: 。
(5)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g)
已知:①FeO(s) + CO(g) = Fe(s) + CO2(g) △H1=-11KJ/mol
②3Fe2O3(s) + CO(g) = 2Fe3O4(s) + CO2(g) △H2=-47KJ/mol
③Fe3O4(s) + CO(g) = 3FeO(s) + CO2(g) △H3=+19KJ/mol
则反应Fe2O3(s) + 3CO(g)= 2Fe(s)+ 3CO2(g)的△H= 。
氮化硅是一种高温陶瓷材料,结构类似于硅、二氧化硅,它的硬度大,熔点高,化学性质稳定,工业上曾普遍采用高纯硅与纯氮在1300℃反应制得。
(1)根据性质,推测氮化硅的用途是()
| A.制汽轮机叶片 | B.制有色玻璃 |
| C.制永久性模具 | D.制造柴油机 |
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应,试推测该陶瓷被氢氟酸腐蚀的化学方程式_______________________________________。
(3)用四氯化硅在氢气中与氮气反应(加强热)可制得较高纯度的氮化硅,反应的化学方程式为_____________________________________________________。
矿泉水一般是由岩石风化后被地下水溶解其中可溶部分生成的。此处的风化作用是说矿物与H2O和CO2同时作用的过程。案例如钾长石(KAlSi3O8)风化生成高岭土〔Al2Si2O5(OH)4〕,此反应的离子方程式是:2KAlSi3O8+11H2O+2CO2 2K++2
2K++2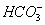 + 4H4SiO4+Al2Si2O5(OH)4,这个反应能发生的原因是_____________。Al2Si2O5(OH)4改写成氧化物的形式为__________________________。
+ 4H4SiO4+Al2Si2O5(OH)4,这个反应能发生的原因是_____________。Al2Si2O5(OH)4改写成氧化物的形式为__________________________。
结构致密的SiO2。二者成分相同,结构不同,化学性质相同,物理性质上表现出差别,具有不同的用途。由石英制取硅胶,经历以下三步,试写出每步反应的化学方程式(是离子反应的,写出离子方程式)。
(1)用NaOH(aq)溶解石英:_________________。
(2)过滤,向滤液中加入盐酸,至沉淀不再产生:_________________。
(3)微热,浓缩硅酸溶液,加热蒸干溶液,并使固体完全分解:_________________。
写出硅胶的一种用途:_________________。
三硅酸镁能被用来治疗胃酸过多的胃溃疡,是因为该物质不溶于水,服用后能中和胃酸,作用持久。把三硅酸镁Mg2Si3O8·nH2O改写成氧化物的形式为________________,它中和胃酸(HCl)的化学方程式是_______ ___________________。