设NA为阿伏伽德罗常数的值。下列说正确的是
| A.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA |
| B.室温下,1L pH=13的NaOH溶液中,由水电离的OH- 离子数目为0.1NA |
| C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
| D.5NH4NO3= 2HNO3+ 4N2↑ + 9H2O反应中,生成28g N2时,转移的电子数目为3.75NA |
在标准状况下将1.92g铜粉投入一定量浓HNO3中随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混和气体1.12L,则混和气体中NO的体积为
| A.112mL | B.1008mL | C.224mL | D.448mL |
下列物质之间的转化符合:“甲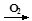 乙
乙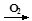 丙
丙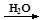 丁”的组合是
丁”的组合是
①Na→NaOH; ②Cu→Cu(OH)2;③S→H2SO4;④NH3→HNO3
| A.①②③ | B.①③④ | C.②③④ | D.全部 |
如右图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了,则液体A和气体B的组合不可能是下列的
| A.氢氧化钠溶液、二氧化碳 | B.水、氨气 |
| C.氢氧化钠溶液、一氧化氮 | D.水、二氧化氮 |
某溶液能与Al粉反应放出H2,该溶液中可能大量共存的离子组是
| A.NH4+、Ba2+、HCO3—、Cl- | B.K+、Al3+、S2-、ClO- |
| C.Na+、Fe3+、Cl-、SO42— | D.NH4+、Mg2+、SO42—、NO3— |
下列方程式不正确的是
| A.向Fe(NO3)2溶液中加稀硝酸:3Fe2++4H++NO3-==3Fe3++NO↑+2H2O |
B.向氯化铵的稀溶液中加入足量NaOH并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| C.向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-==BaSO4↓ |
| D.向稀硝酸中加入铜片:3Cu+8H++2NO3-==3Cu2++2NO↑+4H2O |