22.甲:在试管中加入1 g粉末状大理石,加入4 mol/L盐酸20 mL(过量);
乙:在试管中加入2 g颗粒状大理石,加入4 mol/L盐酸20 mL(过量);
生成体积(折算成标准状况)V(CO2)同反应时间t的关系曲线图合理的是
下列反应中,反应物的用量或浓度改变时,不会改变生成物的是()
| A.铁与硫酸反应 | B.氢氧化钠溶液和CO2反应 |
| C.硫在氧气中燃烧 | D.铜和与硝酸反应 |
下列除杂质的操作中不正确的是()
| A.铁粉中混有铝粉:加入过量烧碱溶液充分反应后过滤 |
| B.FeCl2溶液中混有FeCl3:加入过量铁粉充分反应后过滤 |
| C.Na2CO3固体中混有少量NaHCO3:加入适量NaOH溶液 |
| D.Al(OH)3中混有Mg(OH)2:加入足量烧碱溶液后过滤,向滤液中通入过量CO2后过滤 |
下图装置可用于收集气体X并验证其某些化学性质,
你认为正确的是()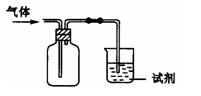
| 选项 |
气体 |
试剂 |
现象 |
结论 |
|
等物质的量的镁和铝混合均匀后,分为等量的四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是( )
| A.3 mol•L-1HCl溶液 | B.3 mol•L-1HNO3溶液 |
| C.8 mol•L-1NaOH溶液 | D.18 mol•L-1 浓H2SO4溶液 |
设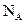 表示阿伏加德罗常数的值,下列叙述正确的()
表示阿伏加德罗常数的值,下列叙述正确的()
A.常温常压下4.6g NO2和N2O4混合气体所含原子总数为0.3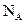 |
B.100mL 2mol/L的NaCl溶液中含NaCl分子数为0.2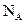 |
C.标准状况下,22.4 L水中含有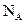 个H2O分子 个H2O分子 |
D.1 mol铁单质参加反应转移电子数一定为2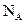 |