5.近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI+3H2O 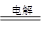 KIO3+3H2↑。下列有关说法不正确的是(相对原子质量:K:39,I:127,O:16)
KIO3+3H2↑。下列有关说法不正确的是(相对原子质量:K:39,I:127,O:16)
| A.电解时,石墨作阴极,不锈钢作阳极 |
| B.电解时,阳极反应是:I――6e-+3H2O=IO3-+6H+ |
| C.当电解过程中转移3mole-时,理论上可制得KIO3 107g |
| D.电解前后溶液的pH几乎不变 |
下列电池工作时,O2在正极放电的是
 |
 |
 |
 |
| A.甲醇燃料电池 |
B.镍镉电池 |
C.锌锰电池 |
D.铅蓄电池 |
下列说法正确的是
| A.放热反应都是自发,吸热反应都非自发 |
| B.熵增反应不一定自发,但自发反应熵一定增大 |
| C.自发反应是不可逆反应 |
| D.判断反应进行的方向,应综合考虑体系的焓变和熵变 |
还原2.4×10-3mol〔 XO(OH)〕2+到X元素的低价态时,需消耗30mL0.2mol·L-1的亚硫
酸钠(Na2SO3)溶液,则在此反应中X元素的低价态为
| A.0价 | B.+1价 | C.-1价 | D.-2价 |
常温下,下列三个反应均能发生:X2+2W2+===2X-+2W3+; Z2+2X-===2Z-+X2;
2W3++2Y-===2W2++Y2。则在相同条件下,下列三个反应:①Y2+2X-===2Y-+X2;
②Z2+2Y-===2Z-+Y2; ③2W3++2Z-===2W2++Z2也能发生的是
| A.只有① | B.只有② | C.①和② | D.②和③ |
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:
①加入稍过量的Na2CO3溶液; ②加入稍过量的NaOH溶液;
③加入稍过量的BaCl2 溶液; ④滴入稀盐酸至无气泡产生; ⑤过滤
正确的操作顺序是
| A.③②①⑤④ | B.①②③⑤④ | C.②③①④⑤ | D.③⑤②①④ |