11.在一个容积可变的密闭容器中发生反应:2X(s)+Y(g)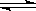 2Z(g)△H>0,欲加快正反应速率且提高Y的转化率,下列方法可行的是
2Z(g)△H>0,欲加快正反应速率且提高Y的转化率,下列方法可行的是
| A.保持容积不变,继续通入Y气体 |
| B.保持容积不变,及时移走Z气体 |
| C.压缩容器,而不改变物质状态 |
| D.保持容积不变,升高温度 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是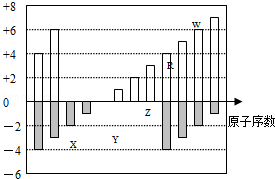
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R>W |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
BeCl2熔点较低,易升华,溶于醇和醚,其化学性质与AlCl3相似。由此可推测BeCl2正确的是
| A.熔融态不导电 | B.水溶液呈中性 |
| C.熔点比BeBr2高 | D.不与氢氧化钠溶液反应 |
下列排序正确的是
| A.酸性:H2CO3<C6H5OH<H3COOH |
| B.碱性:Ba(OH)2<Ca(OH)2<KOH |
| C.熔点:MgBr2<SiCl4<BN |
| D.沸点:PH3<NH3<H2O |
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是
| A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.X的最高价氧化物对应水化物的酸性比W的弱 |
| D.Y的气态简单氢化物的热稳定性比W的强 |
下列有关元素的性质及其递变规律正确的是
| A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| B.第二周期元素从左到右,最高正价从+1递增到+7 |
| C.同主族元素的简单阴离子还原性越强,水解程度越大 |
| D.同周期金属元素的化合价越高,其原子失电子能力越强 |