15.在不同温度下,向2 L密闭容器中加入1 mol NO和1 mol活性炭,发生反应:
2NO(g)+C(s) N2(g)+CO2(g) ΔH=﹣213.5 kJ/mol,达到平衡时的数据如下:
N2(g)+CO2(g) ΔH=﹣213.5 kJ/mol,达到平衡时的数据如下:
| 温度/℃ |
n(活性炭)/mol |
n(CO2)/mol |
| T1 |
0. 70 |
_______ |
| T2 |
_______ |
0.25 |
下列说法不正确的是
A.上述信息可推知:T1<T2
B.T1℃时,该反应的平衡常数K=9/16
C.T2℃时,若反应达平衡后再缩小容器的体积,c (N2) :c (NO)不变
D.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如下图所示,则溶液中c(Cl¯)与c(SO42¯)之比为()
| A.1∶1 | B.2∶3 | C.3∶2 | D.2∶1 |
某pH=1的X溶液中可能含有Fe2+、A13+、NH4+、CO32―、SO32―、SO42―、C1―中的若干种,现取X溶 液进行连续实验,实验过程及产物如下:
下列说法正确的是()
| A.气体A是NO2 |
| B.X中肯定存在Fe2+、A13+、NH4+、SO42― |
| C.溶液E和气体F不能发生化学反应 |
| D.X中不能确定的离子是 A13+和C1― |
某碱金属R与其氧化物R2O的混合物2.16g,跟足量水充分反应后,将所得溶液蒸干,得固体3.2 g,由此判定金属是()
| A.锂 | B.钠 | C.钾 | D.铷 |
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中不正确 的是()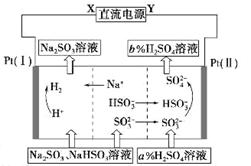
| A.X为直流电源的负极,Y为直流电源的正极 |
| B.阳极区pH增大 |
| C.图中的b>a |
| D.该过程中的产品主要为H2SO4和H2 |
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法正确的是()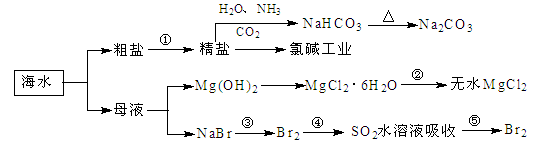
| A.制取NaHCO3的反应是利用其溶解度小于NaCl |
| B.用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C.在第③、④、⑤步骤中,溴元素均被氧化 |
| D.工业上通过电解饱和MgCl2溶液制取金属镁 |