在隔绝空气的情况下,9.2 g铁、镁、铝混合物溶解在一定量某浓度的稀硝酸中,当金属完全溶解后收集到4.48 L(标准状况下)NO气体。在反应后的溶液中加入足量的烧碱溶液,可生成氢氧化物沉淀的质量为
| A.18.6 g | B.20 g | C.19.4 g | D.24 g |
FeCO3与砂糖混用可以作补血剂,实验室里制备FeCO3的流程如图所示,下列说法错误的是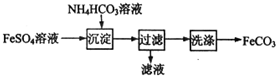
| A.可利用KSCN溶液检验FeSO4溶液是否变质 |
| B.沉淀过程中有CO2气体放出 |
| C.过滤搡作的常用玻璃仪器有烧杯、漏斗和玻璃棒 |
| D.产品FeCO3在空气中高温分解可得到纯净的FeO |
下列除杂方案错误的是
| 选项 |
被提纯的物质 |
杂质 |
除杂试剂 |
| A |
FeCl3(aq) |
Al3+(aq) |
NaOH溶液、盐酸 |
| B |
AlCl3(aq) |
Cu2+ |
Al粉 |
| C |
NaHCO3(aq) |
Na2CO3(aq) |
CO2气体 |
| D |
FeCl3(aq) |
Cu2+ |
Fe粉 |
下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是
①NaHCO3②Al2O3③Al(OH)3④Al ⑤Na2CO3
| A.①③④ | B.②③④⑤ | C.①②③④ | D.全部 |
某溶液中有Fe3+、Mg2+、Fe2+和Na+四种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量盐酸,溶液中大量减小的阳离子是
| A.Fe3+ | B.Mg2+ | C.Na+ | D.Fe2+ |
下列有关硅及其化合物的说法中正确的是
| A.陶瓷、玻璃、水泥容器都能贮存氢氟酸 |
| B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞的试剂瓶中 |
| C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2 |
D.由Na2CO3+SiO2 CO2+Na2SiO3可知硅酸的酸性大于碳酸 CO2+Na2SiO3可知硅酸的酸性大于碳酸 |