某溶液含有①NO3-、②HCO3-、③SO32-、④CO32-、⑤SO42—五种阴离子。现向其中加入少量的Na2O2固体后,溶液中离子浓度增大的是(设溶液体积无变化)
| A.① | B.④ | C.①④⑤ | D.④⑤ |
用NA表示阿伏加德罗常数的数值,下列说法不正确的是 ( )
| A.2.3g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA |
| B.1molNa2CO3晶体中含CO32ˉ数目一定为NA |
| C.常温常压下,92g的NO2和N2O4混合气体中含有原子数为6 NA |
| D.惰性电极电解食盐水,若电路中通过NA个电子,则阳极产生气体11.2L |
下列说法正确的是 ( )
| A.从海水中提取物质都必须通过化学反应才能实现 |
| B.二氧化硫可用于消毒杀菌和漂白纸张草帽等 |
| C.过氧化钠、烧碱、纯碱分别属于碱性氧化物、碱、盐 |
| D.Na、Al、Cu可以分别用热还原法、热分解法和电解冶炼法得到 |
如图为一原电池的结构示意图,下列说法中,不正确的是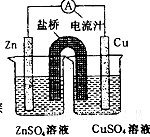
| A.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu |
| B.原电池工作时,Zn电极流出电子,发生氧化反应 |
| C.原电池工作时,铜电极上发生氧化反应,CuSO4溶液蓝色变深 |
| D.盐桥中阳离子流向CuSO4溶液中 |
将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O,下列判断合理的是
| A.Fe(NO3)x中的x为2 |
| B.磁性氧化铁中的铁元素全部被氧化 |
| C.稀HNO3在反应中只作氧化剂 |
| D.反应中每生成0.4 mol还原产物,就有1.2 mol电子转移 |
下列有关热化学方程式书写及对应表述均正确的是
| A.密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量。则Fe(s)+S(s)=FeS(s)△H=-95.6kJ/mol |
| B.稀醋酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol |
| C.已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5kJ/mol |
| D.已知2C(s)+O2(g)=2CO(g)△H=-221kJ/mol,则可知C的燃烧热△H=-110.5kJ/L |