已知,在热的碱性溶液中NaClO能发生如下反应:3NaClO—→2NaCl+NaClO3。在相同条件下NaClO2也能发生类似反应,其最终产物是
| A.NaCl、NaClO | B.NaCl、NaClO3 |
| C.NaClO、NaClO3 | D.NaClO3、NaClO4 |
下列各组离子能在指定环境中大量共存的是( )
A.在c(HCO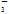 )=0.1 mol·L-1的溶液中:NH )=0.1 mol·L-1的溶液中:NH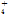 、AlO 、AlO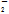 、Cl-、NO 、Cl-、NO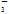 |
B.在由水电离出的c(H+)=1×10-12 mol·L-1的溶液中:Fe2+、ClO-、Na+、SO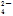 |
C.在加入铝粉产生H2的溶液中:SO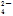 、NO 、NO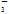 、Na+、NH 、Na+、NH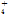 |
D.在使红色石蕊试纸变蓝的溶液中:SO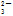 、CO 、CO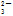 、Na+、K+ 、Na+、K+ |
下列有关说法中,正确的是( )
①钢较纯铁不易生锈;
②冶炼铝和钠都可以用电解法;
③KSCN溶液可以检验Fe3+离子;
④缺钙会引起骨质疏松,缺铁会引起贫血;
⑤青铜、不锈钢、硬铝都是合金
| A.①②③④⑤ |
| B.②③④⑤ |
| C.①③④ |
| D.①②④⑤ |
化学与生活、社会密切相关,下列说法不正确的是( )
| A.碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜锡合金 |
| B.氨很容易液化,液氨气化吸收大量的热,所以液氨常用作致冷剂 |
| C.Al2O3用作耐火材料、Al(OH)3用作阻燃剂 |
| D.SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 |
工业上常用FeCl3溶液与铜反应制作印刷电路板。该反应的化学方程式为:2FeCl3+Cu =2FeCl2+CuCl2。取上述反应后溶液10 mL进行分析,测得其中c(Fe3+)为1mol·L—1。向其中加入足量的硝酸银溶液,过滤、干燥,可得到沉淀l7.22g。则上述反应后的10mL溶液中c(Cu2+)为
| A.0.5mol·L—1 | B.1.5 mol·L—1 | C.0.4 mol·L—1 | D.0.25 mol·L—1 |
下列实验操作中正确的是
| A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B.蒸馏时,温度计水银球靠近蒸馏烧瓶的底部 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.检验溶液中是否含有NH4+:取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |