镁铝合金5.1 g溶于300mL2mol/L的HCl,在标准状况下放出气体的体积为5.6L。向反应后的溶液中加入足量氨水,产生沉淀的质量为
| A.5.1g | B.10.2g | C.13.6g | D.15.3g |
下表中所示物质或概念间的从属关系符合图-6的是()
| X |
Y |
Z |
|
| A |
钠元素 |
主族元素 |
短周期元素 |
| B |
氢氧化铁 |
胶体 |
分散系 |
| C |
电解质 |
化合物 |
纯净物 |
| D |
置换反应 |
氧化还原反应 |
放热反应 |
水的电离平衡曲线如右图所示,下列说法不正确的是()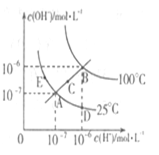
| A.图中五点Kw间的关系:B>C>A=D=E |
| B.若从A点到D点,可采用在水中加入少量酸的方法 |
| C.若从A点到C点,可采用温度不变时在水中加入适量NH4C1固体的方法 |
| D.若处在B点时,将pH =2的硫酸溶液与pH = 10的KOH溶液等体积混合,所得溶液呈中性 |
在等体积的NaCl、MgCl2、AlCl3三种溶液中,分别加入等量的AgNO3溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为()
| A.1:2:3 | B.3:2:1 | C.1:1:1 | D.6:3:2 |
下列除杂的操作方法正确的是()
| A.NO中有少量的NO2:用水洗涤后再干燥 |
| B.食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干 |
| C.Cl2中有少量的HCl:通过氢氧化钠溶液洗气 |
| D.CO2中混有少量的SO2气体:通过饱和NaHSO3溶液洗气 |
下列有关无机非金属材料的说法中,不正确的是()
| A.高纯硅可用于制造半导体材料 |
| B.SiO2制成的玻璃纤维,由于导电能力强而被用于制造光缆 |
| C.玻璃、水泥和陶瓷,其成分均含有硅酸盐 |
| D.Si3N4是一种新型无机非金属材料,可应用于制造发动机 |