下列溶液中微粒的物质的量浓度关系不正确的是
| A.室温下,向0.01mol/LNH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c (SO42-)>c(NH4+)>c(OH-)=c(H+) |
| B.0.4 mol/L HCl与0.1 mol/L NaAlO2等体积混合,所得溶液中:c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-) |
| C.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2 c(H2CO3); |
D.25℃时,pH=4.75、浓度均为0.1mol/L的CH3COOH、CH3COONa混合溶液c(Na+)>c(CH3COO-)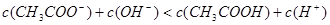 |
相同质量的两份铝,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压下的体积比为()
| A.1:1 | B.1:6 | C.2: 3 | D.3:2 |
2.1 g CO在足量的O2中充分燃烧,然后通过足量的Na2O2固体,固体增加的质量为()
| A.7.2 g | B.4.2 g | C.3.3 g | D.2.1 g |
只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3五种溶液, 这种试剂是()
| A.KSCN | B.H2SO4 | C.NaOH | D.AgNO3 |
向下列各物质的水溶液中滴加稀硫酸或MgCI2溶液时,均有白色沉淀生成的是
| A.BaCI2 | B.Ba(OH)2 | C.Na2CO3 | D.KOH |
把少量废铁屑溶于过量的稀硫酸,过滤,除去杂质,在滤液中加入适量硝酸,再加入过量的氨水,有红褐色沉淀生成。过滤,加热沉淀物至质量不再发生变化,得到红棕色的残渣。上述沉淀和残渣分别为()
| A.Fe2O3;Fe(OH)3 | B.Fe(OH)3;Fe2O3 |
| C.Fe(OH)2;FeO | D.Fe(OH)3;Fe3O4 |