下列与金属腐蚀有关的说法,正确的是 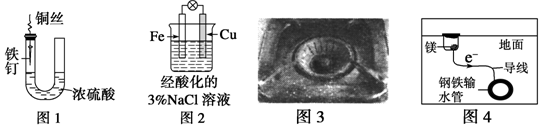
| A.图1中,铁钉易被腐蚀 |
| B.图2中,滴加少量KSCN溶液,溶液变为血红色 |
| C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 |
| D.图4中, 用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
已知:在100℃时,纯水的c(H+)为1×10—6,此时将pH=12的NaOH溶液V1 L与pH=l的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1∶V2为
| A.1∶9 | B.10∶1 | C.9∶1 | D.1∶10 |
下图是电解NaCl溶液(加有酚酞)装置,其中c、d为石墨电极。下列有关的判断正确的是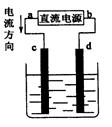
| A.a为负极、d为阳极 |
| B.c电极上的电极反应式为:2H+ + 2e一= 2H2↑ |
| C.电解过程中,d电极附近溶液变红 |
| D.电解过程中,氯离子浓度不变 |
在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有
| A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I- |
| B.pH值为1的溶液:Cu2+、Na+ 、Mg2+、NO3- |
| C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| D.所含溶质为Na2SO4的溶液:K+ 、CO32-、NO3-、Al3+ |
将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经2s后测得SO3的浓度为0.6mol·L-1,下列说法中正确的是
①用O2表示的反应的平均速率为0.6mol·L-1·s-1
②用SO2表示的反应的平均速率为0.3mol·L-1·s-1
③2s时SO2的转化率为15%
④2s时O2的浓度为0.7mol·L-1
| A.①③ | B.①④ | C.②③ | D.②④ |
一定条件下,某反应达到平衡,其平衡常数为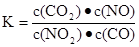 恒容时,升高温度,混合气体的颜色加深,下列说法正确的是
恒容时,升高温度,混合气体的颜色加深,下列说法正确的是
| A.该反应的化学方程式为:NO2+CO===CO2+NO |
| B.该反应的焓变为负值 |
| C.升高温度,正反应速率减小 |
| D.恒温时,增大压强,颜色加深,因平衡左移 |