常温下,下列溶液中的离子浓度关系正确的是
| A.pH =3的醋酸溶液中:c(H+)=c(CH3COO-)=3.0mol•L-1 |
| B.Na2S溶液中:c(Na+)>c(HS-)>c(OH-)>c(H2S) |
| C.pH =2的盐酸与pH =12的氨水等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |
下列有机物能与金属Na反应生成H2的是
| A.乙醇 | B.苯酚 | C.氯苯 | D.乙醚 |
相同物质的量的下列各烃,完全燃烧消耗氧气最多的是
| A.C2H4 | B.C2H2 | C.C3H4 | D.C2H6 |
下列化合物中,既能发生消去反应,又能发生水解反应的是
| A.氯仿 | B.1-氯丙烷 |
| C.2-丁醇 | D.2-甲基-2-溴丙烷 |
下列有关有机物的实验操作、现象或结论不正确的是
| A.提纯含有杂质的工业乙醇,常用的方法是蒸馏 |
| B.常温下,将二氧化碳通入苯酚钠溶液,溶液会变浑浊 |
| C.混有泥沙的苯甲酸,除去杂质的方法是将其溶解后过滤,再蒸发结晶即可 |
| D.苯和苯酚稀溶液分别与浓溴水混合,后者产生白色沉淀 |
下列有机物中,不属于醇类的是
A.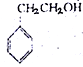 |
B.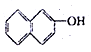 |
C.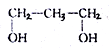 |
D.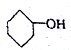 |