在强碱性的无色溶液中,一定可以大量共存的离子组是
| A.NH4+、Na+ 、NO3- 、Cl- | B.K+ 、Ba2+ 、Cl- 、NO3- |
| C.K+ 、Na+ 、H+、SO42- | D.Na+、HS-、Cl-、NO3- |
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上s、p电子数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
| A.X元素的氢化物的水溶液显碱性 |
| B.Z元素的离子半径大于W元素的离子半径 |
| C.Z元素的单质在一定条件下能与X元素的单质反应 |
| D.Y元素最高价氧化物的晶体具有很高的熔点和沸点 |
同周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,Z原子比X原子的核外电子数多4。下列说法正确的是
| A.W、Y、Z的电负性大小顺序一定是Z>Y>W |
| B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C.Y、Z形成的分子的空间构型可能是正四面体 |
| D.WY2分子中σ键与π键的数目之比是2:1 |
短周期元素R、T、Q、W在元素周期表中的相对位置如右下图所示,其中 T 所处的周期序数与族序数相等。下列判断不正确的是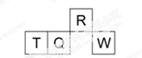
| A.最简单气态氢化物的热稳定性:R > Q |
| B.最高价氧化物对应水化物的酸性:Q < W |
| C.原子半径:T > Q > R |
| D.含 T 的盐溶液一定显酸性 |
四种短周期元素在周期表中的位置如图,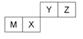 其中只有M为金属元素。下列说法不正确的是
其中只有M为金属元素。下列说法不正确的是
| A.原子半径Z < M |
| B.Y的最离价氧化物对应水化物的酸性比X 的弱 |
| C.X 的最简单气态氢化物的热稳定性比Z的小 |
| D.Z位于元索周期表中第2 周期、第ⅥA族 |
五种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知
| W |
X |
|
| Y |
Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性