用NA表示阿伏加德罗常数,下列有关说法正确的是
| A.1 L lmol·L-1的氨水中,含有的NH3与NH3·H2O分子的总数为NA |
| B.标准状况下,2.24 L SO3含有的原子数为0.4NA |
| C.1 molNa2O2与足量的水反应,转移的电子数为2NA |
| D.0.1molNa和氧气在一定条件下反应生成3.5g氧化物时,失去的电子数为0.1NA |
出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。下列说法不正确的是
| A.锡青铜的熔点比纯铜高 |
| B.在自然环境中,锡青铜中的锡可对铜起保护作用 |
| C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快 |
| D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程 |
用下列装置能达到有关实验目的的是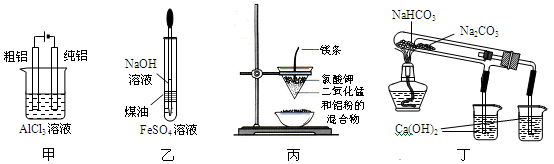
| A.用甲图装置电解精炼铝 |
| B.用乙图装置制备Fe(OH)2 |
| C.用丙图装置制取金属锰 |
| D.用丁图装置比较NaHCO3和Na2CO3的热稳定性 |
下列反应的离子方程式正确的是
| A.澄清石灰水中滴加少量的小苏打溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
| B.铵明矾[NH4Al(SO4)2·12H2O]溶液中加入过量Ba(OH)2溶液: Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| C.过氧化钠和水反应:2O22-+2H2O=4OH-+O2↑ |
| D.H2O2溶液中滴加酸性KMnO4溶液: 2 MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.常温下,2.24LN2和O2的混合气体所含原子数为0.2NA |
| B.常温下,pH=2的醋酸溶液中所含有的H+数为0.01NA |
| C.标准状况下,30g NO和16g O2混合所生成的气体分子数大于NA |
| D.标准状况下,6.72L CO2中所含的共用电子对数为1.2NA |
A、B、C、D为四种短周期主族元素,且原子序数依次增大。已知A的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子。下列说法正确的是
A.原子半径:C>A
B.离子半径:D3+>B2-
C.非金属性:A>B
D.最高价氧化物对应水化物的碱性:C < D