用下图装置(夹持、加热装置已略)进行实验,由②中现象不能证实①中反应发生的是
| |
①中实验 |
②中现象 |
| A |
铁粉与水蒸气加热 |
肥皂水冒泡 |
| B |
加热NH4Cl和Ca(OH)2混合物 |
酚酞溶液变红 |
| C |
加热CaCO3固体 |
澄清石灰水变浑浊 |
| D |
加热KClO3和MnO2的混合物 |
用带火星的木条伸入试管②,木条复燃 |
在密闭容器中进行可逆反应,A跟B反应生成C,反应速率 、
、 、
、 之间存在以下关系:
之间存在以下关系: ,
, ,则该反应可以表示为
,则该反应可以表示为
A.A+B C C |
B.2A+2B 3C 3C |
C.A+3B 2C 2C |
D.3A+B 2C 2C |
恒温恒容条件下,能使

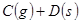 正反应速率加快的是
正反应速率加快的是
| A.减少C或D的物质的量 |
| B.体积不变充入氦气使压强增大 |
| C.减少B的物质的量 |
| D.增大A或B的物质的量 |
取两个相同容积的密闭恒容容器,在A容器中充入0.2molN2O4,B容器中充入0.2molHI气体,在一定温度下反应分别达到平衡,测得N2O4和HI的分解率分别为a(A)和a(B)。在该平衡体系中再分别充入0.2molN2O4和0.2molHI,当反应重新达到平衡时,测得N2O4和HI的分解率分别为a′(A)和a′(B)。下列判断一定正确的是
A.a(A)>a′(A) a(B)<a′(B) B. a(A)>a′(A) a(B)= a′(B)
C.a(A)<a′(A) a(B)<a′(B) D. a(A)= a′(A) a(B)>a′(B)
下列叙述正确的是
| A.醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
| B.在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
| D.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(CH3COO-)<c(Na+) |
“茶倍健”牙膏中含有茶多酚,期中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中正确的是
A.分子式为C15H12O7
B.EGC可在强碱的醇溶液中发生消去反应
C.1molEGC最多消耗6molNaOH
D.1molEGC可与4molBr2发生取代反应