设NA为阿伏加德罗常数,下列叙述正确的是
| A.2.4g Mg在空气中完全燃烧失去的电子数为0.2NA |
| B.22.4 L氯气与过量的铁完全反应,转移电子数为2NA |
| C.含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2︰3 |
| D.1.8g 1H218O中含有的电子数为NA |
某同学按右图所示的装置进行实验。 A、B为两种常见金属,它们的硫酸盐可溶于水。当 K 闭合时,在交换膜处 SO42一从右向左移动。下列分析正确的是( )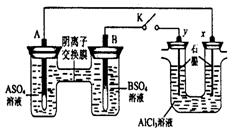
A.溶液中(A2+)浓度减小
B.B的电极反应:B-2eˉ=B2+
C.反应初期,x 电极周围出现白色胶状沉淀,不久沉淀溶解
D.y 电极上有 H2产生,发生还原反应
下列叙述正确的是()
| A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| B.X、Y均为短周期元素,其简单离子mXa+与nYb-的电子层结构相同,则m+a=n-b。 |
| C.结合质子(H+)能力:OH->CH3COO->Cl- |
| D.F、Cl、Br的最外层电子数都是7,次外层电子数都是8 |
如图,木炭与浓硫酸共热产生的气体x和铜跟浓硝酸反应产生的气体y同时通入盛有过量M的洗气瓶中,下列说法正确的是 ()  (
(
| A.若M为BaCl2溶液,则洗气瓶中会产生BaCO3和BaSO3沉淀 |
| B.若M为Ba(OH)2溶液,洗气瓶中只会产生BaCO3沉淀 |
C.若M为KI淀粉溶液,洗气瓶中溶液一定会出现蓝色 |
| D.若M为水,在z导管口有红棕色气体出现 |
T℃时,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图2所示:下列描述正确的是()
| A.平衡时X、Y的转化率相同 |
| B.T℃时,若起始时X为0.71mol,Y为1.00 mol,则平衡时Y的转化率约为60% |
C.T℃时,该反应的化学方程式为:X(g)+Y(g)  2Z(g),平衡常数K=40 2Z(g),平衡常数K=40 |
| D.达到平衡后,将容器体积压缩为1 L,平衡向正反应方向移动 |
下列反应的离子方程式中正确的是 ()
| A.用侯氏制碱法制得NaHCO3:Na++NH3+CO2+H2O = NaHCO3↓+NH4+ |
B.亚硫酸氢钠水解:HSO3-+H2O  SO32-+H3O+ SO32-+H3O+ |
| C.苯酚钠的水溶液中通入少量的CO2:2C6H5O- + CO2 + H2O → 2C6H5OH + HCO3- |
| D.甲醇、O2和KOH溶液组成的燃料电池的负极反应:CH3OH+H2O-6e-= CO2↑+6H+ |